题目内容
(2012?阜新)某兴趣小组同学为了验证铁和铜的金属活动性强弱,进行 了如下的实验探究,请你回答有关问题.
[实验探究]
(1)甲同学设计的实验方案:取用砂纸打磨过的铁丝插入到盛有硫酸铜溶液的试管中,过一会儿取出铁丝,观察到铁丝表面
(2)乙同学设计的方案:(实验中所用铜片,铁片大小形状相同)
[讨论交流]实验前乙同学在配制10%的稀盐酸时,用到的仪器有烧杯、量筒、胶头滴管,还缺少的一种仪器是
[反思评价]
(1)你认为乙同学的方案
①
②
[拓展应用]农药波尔多液的主要成分是硫酸铜,不能用铁制容器盛放 波尔多液的原因是:
[实验探究]
(1)甲同学设计的实验方案:取用砂纸打磨过的铁丝插入到盛有硫酸铜溶液的试管中,过一会儿取出铁丝,观察到铁丝表面
覆盖一层红色物质
覆盖一层红色物质
得出结论铁比铜活动性强.(2)乙同学设计的方案:(实验中所用铜片,铁片大小形状相同)
| 实验步骤 | 实验现象 | 实验结论 |
 |
铜片的表面无气泡产生 铁片的表面有气泡产生 |
铁比铜活动性强 |
玻璃棒
玻璃棒
.在量取蒸馏水体积时,若仰视读数,则会导致盐酸的溶质质量分数<
<
10%(填“>”“<”、“=”)[反思评价]
(1)你认为乙同学的方案
不合理
不合理
(填“合理”或“不合理”),理由 是:选择的酸不同
选择的酸不同
(2)通过上述实验可知,比较金属活动性强弱的方法有两种①
利用金属与酸反应比较金属活动性强弱
利用金属与酸反应比较金属活动性强弱
②
利用金属与盐溶液反应比较金属活动性强弱
利用金属与盐溶液反应比较金属活动性强弱
[拓展应用]农药波尔多液的主要成分是硫酸铜,不能用铁制容器盛放 波尔多液的原因是:
Fe+CuSO4=Cu+FeSO4
Fe+CuSO4=Cu+FeSO4
(用化学方程式表示)分析:本题中,题目首先给出了两个实验探究方案,同学们可以根据已有的知识和题目给出的信息,就能够很快的解决.甲同学设计的实验方案:取用砂纸打磨过的铁丝插入到盛有硫酸铜溶液的试管中,过一会儿取出铁丝,观察到铁丝表面覆盖一层红色物质,得出结论铁比铜活泼;配制10%的稀盐酸时,用到的仪器有烧杯、量筒、胶头滴管、玻璃棒;在量取蒸馏水体积时,若仰视读数,水会量多了,则会导致盐酸的溶质质量分数小于10%;我认为乙同学的方案不合理,因为选择的酸不同,控制变量法只能控制一个变量;通过上述实验可知,比较金属活动性强弱的方法有两种:利用金属与酸反应比较金属活动性强弱;利用金属与盐溶液反应比较金属活动性强弱 (或利用金属与金属的化合物溶液反应比较金属活动性强弱 );不能用铁制容器盛放波尔多液的原因是:铁与硫酸铜溶液反应生成硫酸亚铁和铜.
解答:解:[实验探究]甲同学设计的实验方案:取用砂纸打磨过的铁丝插入到盛有硫酸铜溶液的试管中,过一会儿取出铁丝,观察到铁丝表面覆盖一层红色物质,得出结论铁比铜活泼;故答案为:覆盖一层红色物质
[讨论交流]配制10%的稀盐酸时,用到的仪器有烧杯、量筒、胶头滴管、玻璃棒;在量取蒸馏水体积时,若仰视读数,水会量多了,则会导致盐酸的溶质质量分数小于10%;故答案为:玻璃棒;<
[反思评价](1)我认为乙同学的方案不合理,因为选择的酸不同,控制变量法只能控制一个变量;故答案为:不合理 选择的酸不同
(2)通过上述实验可知,比较金属活动性强弱的方法有两种:利用金属与酸反应比较金属活动性强弱;利用金属与盐溶液反应比较金属活动性强弱 (或利用金属与金属的化合物溶液反应比较金属活动性强弱 );故答案为:①利用金属与酸反应比较金属活动性强弱; ②利用金属与盐溶液反应比较金属活动性强弱 (或利用金属与金属的化合物溶液反应比较金属活动性强弱 )
[拓展应用]不能用铁制容器盛放波尔多液的原因是:铁与硫酸铜溶液反应生成硫酸亚铁和铜,故答案为:Fe+CuSO4=Cu+FeSO4
[讨论交流]配制10%的稀盐酸时,用到的仪器有烧杯、量筒、胶头滴管、玻璃棒;在量取蒸馏水体积时,若仰视读数,水会量多了,则会导致盐酸的溶质质量分数小于10%;故答案为:玻璃棒;<
[反思评价](1)我认为乙同学的方案不合理,因为选择的酸不同,控制变量法只能控制一个变量;故答案为:不合理 选择的酸不同
(2)通过上述实验可知,比较金属活动性强弱的方法有两种:利用金属与酸反应比较金属活动性强弱;利用金属与盐溶液反应比较金属活动性强弱 (或利用金属与金属的化合物溶液反应比较金属活动性强弱 );故答案为:①利用金属与酸反应比较金属活动性强弱; ②利用金属与盐溶液反应比较金属活动性强弱 (或利用金属与金属的化合物溶液反应比较金属活动性强弱 )
[拓展应用]不能用铁制容器盛放波尔多液的原因是:铁与硫酸铜溶液反应生成硫酸亚铁和铜,故答案为:Fe+CuSO4=Cu+FeSO4
点评:金属的活动性顺序是中考的重点内容之一,本题既考查了实验现象的描述、化学方程式的书写,又考查了学生的实验设计能力,综合性比较强,同学们要认真掌握.本考点经常出现在选择题、填空题和实验题中.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
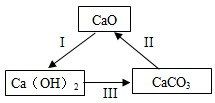 (2012?阜新)归纳和总结是学习化学的重要方法.某校化学小组的同学在复习CaO、Ca(OH)2、CaCO3的化学性质时,归纳出他们之间的转化关系.
(2012?阜新)归纳和总结是学习化学的重要方法.某校化学小组的同学在复习CaO、Ca(OH)2、CaCO3的化学性质时,归纳出他们之间的转化关系.
