题目内容
【题目】人类的生产生活离不开金属。
(1)在地壳里含量最多的金属元素是 ____________(填元素符号) 。
(2)下列铜制品的用途中,利用金属导电性的是 ____________(填字母)。
A 铜火锅 B 铜导线 C 铜 钟 D 铜 钱
(3)下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝。金属大规模被使用的先后顺序跟_______(填字母)关系最大。
A 地壳中金属元素的含量 B 金属的导电性 C 金属的活动性
(4)现有一包由 5.6 g 铁、7.2 g 镁、1.0 g 碳混合而成的粉末,把它加入一定量的氯化铜溶液中。写出铁和氯化铜溶液反应的化学方程式 ____________,实验结束后,测得剩余固体中含有三种物质。则剩余固体的质量不可能是 ____________(填字母)。
A 26.2 g B 26.6 g C 26.0 g D 25.8 g
【答案】Al B C ![]() B
B
【解析】
(1)在地壳里含量最多的金属元素是铝元素,符号为:Al。
(2)A、铜火锅利用铜的导热性;
B、铜导线利用铜的导电性;
C、铜钟是利用铜化学性质稳定;
D 铜钱铜钱是利用了铜的延展性、化学性质稳定;
故填:B;
(3)下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝,故金属大规模被使用的先后顺序跟金属的活动性有关,故填:C;
(4)铁和氯化铜溶液反应生成氯化亚铁和铜,反应的化学方程式为![]() ,实验结束后,测得剩余固体中含有三种物质,则三种物质是不能反应的碳、反应生成的铜和没有或部分反应的铁;
,实验结束后,测得剩余固体中含有三种物质,则三种物质是不能反应的碳、反应生成的铜和没有或部分反应的铁;
设铁完全反应,对应质量关系:
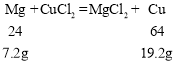
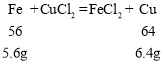
剩余固体质量:1.0g+6.4g+19.2g=26.6g;
设铁没有反应,剩余固体质量:1.0g+5.6g+19.2g=25.8g,
由以上分析可知,剩余固体的质量大于或等于25.8g,小于26.6g,即剩余固体的质量不可能是26.6g。
故选:B。

【题目】甲、乙、丙、丁四种物质的相互反应关系如图所示, 下列选项符合对应反应关系的是
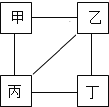
选项 | A | B | C | D | |
物 质 | 甲 | Ca(OH)2 | CO2 | H2 | Fe |
乙 | Na2CO3 | NaOH | O2 | HCl | |
丙 | H2SO4 | CaCl2 | CuO | CuSO4 | |
丁 | BaCl2 | AgNO3 | HCl | NaOH | |
A.AB.BC.CD.D