题目内容
【题目】下图是实验室常用的实验装置,请回答下列问题。
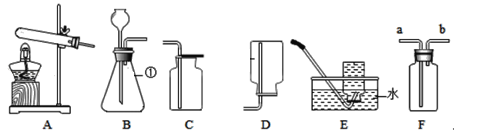
(1)写出仪器①的名称___________ 。
(2)实验室用高锰酸钾制氧气的化学方程式为____________,选择的发生装置是________(填序号),若要收集一瓶供铁丝燃烧实验用的氧气,选择_______(填序号)装置收集氧气比较方便快捷。
(3)实验室用锌粒和稀盐酸制氢气,发生反应的化学方程式为_________。若要利用F装置收集氢气,则气体应从________端通入;若要检验氢气中是否含有氯化氢气体,可选用下列物质中的__________进行检验。
A 石灰浆悬浊液 B 紫色石蕊溶液 C AgNO3溶液 D 酚酞溶液
(4)为了证明氢氧化钙溶液与稀盐酸能发生反应,氢氧化钠溶液与二氧化碳也能发生反应。如下图所示进行实验(装置气密性良好,实验前活塞和弹簧夹K处于关闭状态)。
实验一:证明氢氧化钙溶液与稀盐酸发生反应
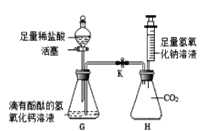
打开分液漏斗的活塞,使稀盐酸逐滴加入G锥形瓶中,观察到________的现象时,关闭活塞,证明氢氧化钙溶液与稀盐酸恰好完全反应。
实验二:证明氢氧化钠与二氧化碳反应
将注射器中的氢氧化钠溶液推入H锥形瓶中,过一段时间后,打开弹簧夹K,观察到的现象是_______,并且溶液呈红色,证明氢氧化钠溶液与二氧化碳确实发生了反应。请写出二氧化碳与氢氧化钠溶液反应的化学方程式是________。锥形瓶H中溶液最后呈红色,为了证明溶液中氢氧化钠有剩余,需进行的操作是:取H中少量溶液于试管中,向其中加足量的CaCl2溶液至不再产生白色沉淀,若溶液仍为红色,则氢氧化钠有剩余。加足量的CaCl2溶液的目的是________。
【答案】锥形瓶 2KMnO4![]() K2MnO4 + MnO2 + O2↑ A E Zn+2HCl=ZnCl2+H2↑ b ABC 溶液由红色恰好变成无色 G中液体进入H中,并生成白色沉淀 CO2 + 2NaOH =Na2CO3 +H2O 除尽Na2CO3溶液,防止对NaOH的检验造成干扰
K2MnO4 + MnO2 + O2↑ A E Zn+2HCl=ZnCl2+H2↑ b ABC 溶液由红色恰好变成无色 G中液体进入H中,并生成白色沉淀 CO2 + 2NaOH =Na2CO3 +H2O 除尽Na2CO3溶液,防止对NaOH的检验造成干扰
【解析】
(1)仪器①的名称是锥形瓶,故填:锥形瓶;
(2)实验室用高锰酸钾制氧气的化学方程式为2KMnO4![]() K2MnO4 + MnO2 + O2↑,根据反应物的状态与反应的条件,选择固固加热型的发生装置,故选A;若要收集一瓶供铁丝燃烧实验用的氧气,选择E装置收集氧气比较方便快捷,因为铁丝与氧气反应时要在集气瓶底留少量水。故填:2KMnO4
K2MnO4 + MnO2 + O2↑,根据反应物的状态与反应的条件,选择固固加热型的发生装置,故选A;若要收集一瓶供铁丝燃烧实验用的氧气,选择E装置收集氧气比较方便快捷,因为铁丝与氧气反应时要在集气瓶底留少量水。故填:2KMnO4![]() K2MnO4 + MnO2 + O2↑ A E;
K2MnO4 + MnO2 + O2↑ A E;
(3)实验室用锌粒和稀盐酸制氢气,发生反应的化学方程式为Zn+2HCl=ZnCl2+H2↑。若要利用F装置收集氢气,因为氢气的密度比空气小,则气体应从b端通入;若要检验氢气中是否含有氯化氢气体,可选硝酸银进行检验,因为硝酸银与氯化氢反应会生成白色沉淀,也可选紫色石蕊试液,紫色石蕊遇氯化氢会变红色,也可选用石灰浆,石灰浆与氯化氢会生成氯化钙溶液,石灰浆悬浊液会变得澄清,故选ABC。故填:Zn+2HCl=ZnCl2+H2↑ b ABC;
(4)实验一:稀盐酸逐滴加入到G瓶中,由于稀盐酸与氢氧化钠反应,生成中性的氯化钠溶液,所以溶液由红色褪为无色,当观察到溶液由红色恰好变成无色时,说明恰好完全反应。
实验二:过一段时间后,打开弹簧夹K,观察到的现象是G中液体进入H中,生成白色沉淀并且溶液呈红色,证明氢氧化钠溶液与二氧化碳确实发生了反应。因为氢氧化钠与二氧化碳反应后容器内压强会减小,所以盐酸与氢氧化钙反应的溶液会变倒吸入H中,氯化钙与碳酸钠反应有碳酸钙白色沉淀产生,最后溶液呈红色说明氢氧化钠可能过量。二氧化碳与氢氧化钠反应的化学方程式为CO2 + 2NaOH =Na2CO3 +H2O;为了证明溶液中氢氧化钠有剩余,向其中加足量的CaCl2溶液的目的是除尽Na2CO3溶液,防止对NaOH的检验造成干扰,因为碳酸钠溶液也呈碱性。故填:溶液由红色恰好变成无色 G中液体进入H中,并生成白色沉淀 CO2 + 2NaOH =Na2CO3 +H2O 除尽Na2CO3溶液,防止对NaOH的检验造成干扰。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案【题目】小王同学在化工颜料店发现一种“银粉”,他猜想该“银粉”可能是银粉、铝粉或锌粉中的一种。为了确定“银粉”的成分,小王将一小包“银粉”带回实验室,并进行了如下实验和相关分析。
(1)取少量“银粉”于试管中,滴加适量盐酸,观察到_____,说明“银粉”一定不是银。
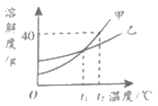
(2)为了进一步确定“银粉”是铝还是锌,小王通过理论计算,获得了铝与足量盐酸反应产生氢气的质量关系,并绘制了铝的图象(如图)。
Zn的质量/g | 0 | 3.25 | m | 9.75 | 13 | 16.25 |
H2的质量/g | 0 | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 |
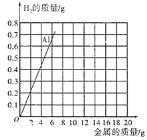
①如表是锌与足量盐酸反应产生氢气的质量关系,请计算表中m的值(利用化学方程式进行计算,写出完整的计算过程)。_____。
②请你在该图中绘制出锌的图象。_____
(3)取1.8g“银粉”(杂质忽略不计)加入到50g稀盐酸中,恰好完全反应,生成氢气0.2g。根据如图可知,“银粉”是_____。