题目内容
用化学方程式解释下列问题:
(1)铝是一种活泼金属,但铝制品却不易锈蚀,原因是: .
(2)常用稀盐酸除去金属铁表面的锈,原因是: .
(3)用含氢氧化镁的药物来治疗胃酸过多,原因是: .
(1)铝是一种活泼金属,但铝制品却不易锈蚀,原因是:
(2)常用稀盐酸除去金属铁表面的锈,原因是:
(3)用含氢氧化镁的药物来治疗胃酸过多,原因是:
考点:书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:(1)铝的化学性质比较活泼,通常情况下能和空气中的氧气反应生成氧化铝;
(2)铁锈的主要成分是氧化铁,能和稀盐酸反应生成氯化铁和水;
(3)氢氧化镁能和胃液中的稀盐酸反应生成氯化镁和水.
(2)铁锈的主要成分是氧化铁,能和稀盐酸反应生成氯化铁和水;
(3)氢氧化镁能和胃液中的稀盐酸反应生成氯化镁和水.
解答:解:(1)铝和氧气反应的化学方程式为:4Al+3O2═2Al2O3;
(2)氧化铁和稀盐酸反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;
(3)氢氧化镁和稀盐酸反应的化学方程式为:Mg(OH)2+2HCl═MgCl2+2H2O.
故填:4Al+3O2═2Al2O3; Fe2O3+6HCl═2FeCl3+3H2O;Mg(OH)2+2HCl═MgCl2+2H2O.
(2)氧化铁和稀盐酸反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;
(3)氢氧化镁和稀盐酸反应的化学方程式为:Mg(OH)2+2HCl═MgCl2+2H2O.
故填:4Al+3O2═2Al2O3; Fe2O3+6HCl═2FeCl3+3H2O;Mg(OH)2+2HCl═MgCl2+2H2O.
点评:书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
 如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )| A、甲的溶解度大于乙的溶解度 |
| B、10℃时甲、乙两种溶液的溶质质量分数相等 |
| C、30℃时甲的饱和溶液的溶质质量分数为60% |
| D、甲、乙两种物质的饱和溶液从30℃降到20℃都会有溶质析出 |
下列物质的鉴别方法错误的是( )
| A、用水鉴别硝酸铵固体和氢氧化钠固体 |
| B、用肥皂水区分硬水和软水 |
| C、用灼烧法鉴别棉纤维和羊毛纤维 |
| D、用酚酞溶液鉴别氢氧化钠和碳酸钠 |
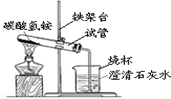 (1)碳酸氢铵失踪之谜[课本p3“观察与思考”]
(1)碳酸氢铵失踪之谜[课本p3“观察与思考”] 化学源于生活,生活中蕴含着许多化学知识.
化学源于生活,生活中蕴含着许多化学知识.