题目内容
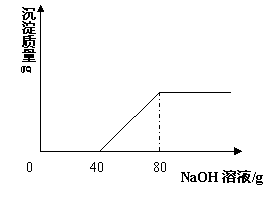
在一烧杯中盛有100 gCuSO4和H2SO4的混合溶液向其中逐渐滴加溶质质量分数为10%的NaOH溶液,混合溶液的质量与所滴入NaOH溶液的质量关系曲线如右图所示。请根据题意回答下列问题![]() :
:
(1)在实验过程中产生沉淀的总质量是______ g。
(2)在实验过程中加入80 gNaOH溶液时所得溶液的pH是___ _7 (填“大于”“小于”或“等于”)。
(3)在实验过程中加入80 gNaOH溶液时,通过计算求此时所得不饱和溶液中溶质的质量分数。(计算结果精确至0.1%)
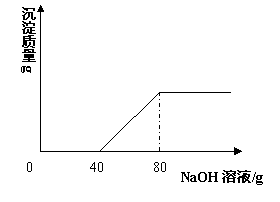
【解析】由图像知,NaOH溶液的质量在0~40 g之间并没有沉淀产生,故先发生的反应是:2NaOH+H2SO4=Na2SO4+2H2O。NaOH溶液的质量在40 g~80 g之间,沉淀质量随着加入Na![]() OH溶液质量的增加而逐渐达到最大值,故发生:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓。在NaOH溶液加至80 g时,两个反应刚好结束,所得溶液中溶质只有硫酸钠且质量为上述两个反应产生的硫酸钠质量之和。
OH溶液质量的增加而逐渐达到最大值,故发生:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓。在NaOH溶液加至80 g时,两个反应刚好结束,所得溶液中溶质只有硫酸钠且质量为上述两个反应产生的硫酸钠质量之和。
答案:(1)4.9 g;(2)等于;
(3)解:设与硫酸反应生成的碳酸钠质量为x,与硫酸铜反应生成的硫酸钠质量为y,
2NaOH+H2SO4=Na2SO4+2H2O
80 142
40 g×10% x
解得:x=7.1 g;
2NaOH + CuSO4 = Na2SO4+ Cu(OH)2↓
80 142
(80 g—40 g)×10% y
解得:y=7.1 g;
不饱和溶液中Na2SO4总质量为: 7.1 g+7.1 g = 14.2 g;
不饱和溶液的质量为: 100 g+80 g-4.9 g = 175.1 g;
所得不饱和溶液中Na2SO4质量分数:![]() ×100%=8.1%。
×100%=8.1%。
答:略。
【易错点点睛】此题较前面两个例题复杂,解题的关键是根据图像的分段,能够意识到反应发生的先后顺序,能够理解几个特殊点的化学含义。在求不饱和溶液中硫酸钠质量时,还可以根据元素守恒思想,建立H2SO4和Na2SO4的对应关系,根据硫酸的总质量一步求出硫酸钠质量。