题目内容
【题目】(1)制取气体是初中化学实验的重要内容,请根据下列装置图回答问题:
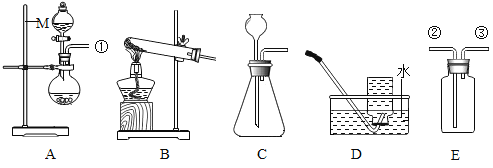
①仪器M的名称是_____;
②实验室用过氧化氢溶液与二氧化锰制备氧气,可选用的发生装置为_____(填字母序号),反应的符号表达式为_____;
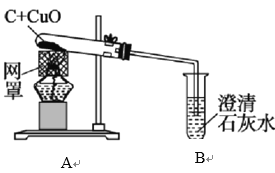
③C装置中的一处明显错误为_____;
④某气体只能用D装置收集,则该气体可能具有的性质为_____(填字母序号);
a.能与水反应
b.能与空气反应
e.密度与空气接近
⑤若用A、E装置制取H2,按气体流向,导管口连接顺序为_____(填序号)。
(2)研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
①(假设)H2O2生成O2的快慢与催化剂种类有关
(实验方案)常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一集气瓶(相同体积)O2所需的时间。
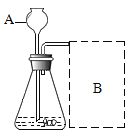
(进行实验)如图是他们进行实验的装置图,气体发生装置中A仪器名称是_____,此实验中B处宜采用的气体收集方法是_____。
(实验记录)
实验编号 | 1 | 2 |
反应物 | 5% H2O2 | 5% H2O2 |
催化剂 | 1g水泥块 | 1gMnO2 |
时间 | 165秒 | 46秒 |
(结论)该探究过程得出的结论是_____。
②(假设)_____;
(实验方案)同温下取2份质量相等、质量分数不同的H2O2溶液,_____结果质量分数大的过氧化氢溶液生成的氧气快,先收集满集气瓶。
【答案】铁架台 A或C  长颈漏斗的下端没有伸入液面以下 bc ①③②(或①③) 锥形瓶 排水法 相同条件下H2O2生成O2的快慢与催化剂的种类有关 H2O2生成O2的快慢与H2O2的质量分数有关 分别加入质量相等的同种催化剂,测量收集一集气瓶(相同体积)气体所需的时间
长颈漏斗的下端没有伸入液面以下 bc ①③②(或①③) 锥形瓶 排水法 相同条件下H2O2生成O2的快慢与催化剂的种类有关 H2O2生成O2的快慢与H2O2的质量分数有关 分别加入质量相等的同种催化剂,测量收集一集气瓶(相同体积)气体所需的时间
【解析】
(1)①仪器M是铁架台;
②用过氧化氢溶液与二氧化锰制取氧气,是液体和固体常温下制取气体,所以选择的发生装置是A或C,反应的符号表达式为
③C装置中的长颈漏斗的下端要伸入液面以下,防止生成的气体从长颈漏斗下端逸出;
④)某气体只能用D装置收集,则该气体可能具有的性质为:①能与空气反应;②密度与空气接近;肯定不与水反应或者易溶于水。故选:bc;
⑤因为氢气的密度比空气小,可用向下排空气法收集,按气体流向,导管口连接顺序为:①③②。
(2)①[进行实验]
A仪器名称是锥形瓶;氧气不易溶于水,且密度比空气大,因此可以采用排水法或向上排空气法收集,相对来说排水法容易准确地判断收集满氧气的时间。
[结论]
根据控制变量法,分析表中的有关数据,可知分别用1g水泥块和1gMnO2做催化剂,来催化反应时所用的时间分别是165s和46s;由此可知,用1gMnO2做催化剂要比用1g水泥块做催化剂时,化学反应速率要快.因此,由实验现象可以得出的实验结论是:H2O2生成氧气的快慢与催化剂种类有关。
②[假设]
可以假设:H2O2生成氧气的快慢与过氧化氢的浓度有关。
[实验方案]
同温下取2份质量相等,质量分数不同的H2O2溶液,分别加入质量相等的同种催化剂,测量收集一试管气体所需的时间,结果质量分数大的过氧化氢溶液生成的氧气快,先收集满.

【题目】维生素C又名抗坏血酸,它能增强人体对疾病的抵抗能力。某化学学习小组对其进行如下研究:
(查阅资料)维生素C常温下为白色晶体,易与氧气、高锰酸钾等物质反应。
Ⅰ.探究维生素C的性质
(进行实验)
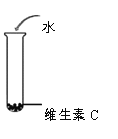
实验序号 | 1-1 | 1-2 | 1-3 | 1-4 |
操作 |
|
|
|
|
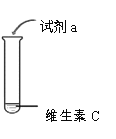
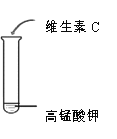
现象 | 白色固体消失,形成溶液 | 溶液变为红色 | …… | 紫色溶液褪色 |
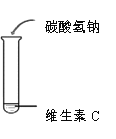
结论 | …… | 维生素C溶液为酸性 | 维生素C能与 碳酸氢钠反应 | 维生素C能与高锰酸钾反应使其溶液褪色 |
(1)由实验1-1现象推测维生素C具有的物理性质是______。
(2)实验1-2中使用的试剂a为_________(填序号,下同)。
A.紫色石蕊试液 B.无色酚酞试液 C.氢氧化钠溶液
(3)实验1-3中实验现象为__________。
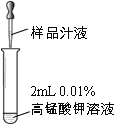
Ⅱ.测定食品中维生素C的含量
(进行实验)
实验序号 | 2-1 | 2-2 | 2-3 | 2-4 | 2-5 | |
实验操作 |
| 鲜榨的猕猴桃汁 | 鲜榨的橙汁 | 鲜榨的西红柿汁 | 加热后冷却至室温的鲜榨西红柿汁 | 放置12小时的西红柿汁 |
紫色溶液褪色时所滴加的样品滴数 | 6 | 8 | 11 | 14 | …… | |
(解释与结论)
(4)实验2-1至2-4中,维生素C的含量最高的是___________。
(5)由实验2-1至2-4可知,影响食品中维生素C含量的因素有_________。
(6)请你推测实验2-5中,紫色溶液褪色时的样品滴数可能为_________。
A.9 B.11 C.15