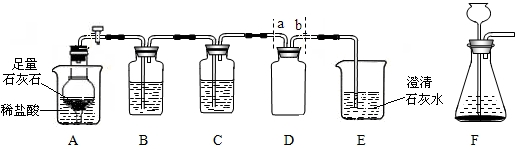
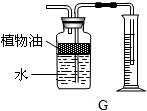
题目内容
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)
则下列分析推理中不正确的是( )
| 50mL | 50mL | 50mL | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
| A、盐酸的物质的量浓度为3.0mol?L |
| B、根据表中数据不能计算出混合物中NaHCO3的质量分数 |
| C、加入混合物9.2g时盐酸过量 |
| D、15.7g混合物恰好与盐酸完全反应 |
分析:A、根据方程式可以看出1mol的盐酸会生成1mol的二氧化碳,通过二氧化碳计算出盐酸的物质的量,在计算出摩尔浓度;
B、根据混合物的质量和二氧化碳的物质的量,可以及计算出碳酸钠的质量,也就可以得出质量分数;
C、根据前面两组中的数据进行分析;
D、根据前面两组中的数据进行分析.
B、根据混合物的质量和二氧化碳的物质的量,可以及计算出碳酸钠的质量,也就可以得出质量分数;
C、根据前面两组中的数据进行分析;
D、根据前面两组中的数据进行分析.
解答:解:NaHCO3+HCl=NaCl+H2O+CO2↑,KHCO3+HCl=KCl+H2O+CO2↑,
A、通过后面的两组数据可以看出,第三组数据中混合物是过量的,盐酸全部参加反应,从上面的方程式可以看出盐酸的物质的量和二氧化碳物质的量是相等的,
二氧化碳物质的量是:
=0.15mol,所以盐酸的物质的量就是0.15mol,摩尔浓度就是:
=3mol/L,故A正确;
B、从前两组中的数据可以看出,二氧化碳的体积增加了
,混合物的质量也需要增加
,第二组中实际参加反应的混合物是13.8克,15.7克的混合物没有反应完,实际盐酸已经不足了,设碳酸氢钠是x克,则碳酸氢钾就是(13.8-x)克,
依据方程式可以看出碳酸氢钠和碳酸氢钾与盐酸物质的量都是1:1,所以碳酸氢钠物质的量是:
,碳酸氢钾物质的量是:
,
+
=0.15
x=6.3克.
质量分数为:
×100%=46%,故B错误;
C、从B中的计算可以看出,50mL盐酸会与13.8克的混合物反应,所以9.2克时盐酸过量,故C正确;
D、从前两组中的数据可以看出,二氧化碳的体积增加了
,混合物的质量也需要增加
,第二组中实际参加反应的混合物是13.8克,故D错误;
故选BD.
A、通过后面的两组数据可以看出,第三组数据中混合物是过量的,盐酸全部参加反应,从上面的方程式可以看出盐酸的物质的量和二氧化碳物质的量是相等的,
二氧化碳物质的量是:
| 3.36 |
| 22.4 |
| 0.15 | ||
|
B、从前两组中的数据可以看出,二氧化碳的体积增加了
| 1 |
| 2 |
| 1 |
| 2 |
依据方程式可以看出碳酸氢钠和碳酸氢钾与盐酸物质的量都是1:1,所以碳酸氢钠物质的量是:
| x |
| 84 |
| 13.8-x |
| 100 |
| x |
| 84 |
| 13.8-x |
| 100 |
x=6.3克.
质量分数为:
| 6.3 |
| 13.8 |
C、从B中的计算可以看出,50mL盐酸会与13.8克的混合物反应,所以9.2克时盐酸过量,故C正确;
D、从前两组中的数据可以看出,二氧化碳的体积增加了
| 1 |
| 2 |
| 1 |
| 2 |
故选BD.
点评:在解此类题时,首先要知道气体的摩尔体积和液体摩尔浓度的计算,然后再结合学过的知识分析解答.

练习册系列答案
相关题目
| 某学生用NaHCO3和KHCO3组成的混合物进行实验,测得如下数据(盐酸质量分数相等)信息: NaHCO3+HCl═NaCl+H2O+CO2↑;KHCO3+HCl═KCl+H2O+CO2↑
|
某学生用NaHCO3和KHCO3组成的混合物进行实验,测得如下数据(盐酸质量分数相等)信息:
NaHCO3+HCl═NaCl+H2O+CO2↑;KHCO3+HCl═KCl+H2O+CO2↑
| 50克盐酸 | 50克盐酸 | 50克盐酸 | |
| 混合物质量 | 9.2克 | 15.7克 | 27.6克 |
| CO2质量 | 4.4克 | 6.6克 | 6.6克 |
- A.盐酸的质量分数为7.3%
- B.加入混合物9.2g时盐酸过量
- C.根据表中数据不能计算出混合物中碳酸氢钠的质量分数
- D.混合物中碳酸氢钠和碳酸氢钾的质量比为1:1
 20、某校在进行“消防演练”时,让学生用干粉灭火器进行灭火训练.化学兴趣小组的同学在老师的指导下,对灭火剂碳酸氢钠(NaHCO3)的灭火原理进行实验探究,请你参与.
20、某校在进行“消防演练”时,让学生用干粉灭火器进行灭火训练.化学兴趣小组的同学在老师的指导下,对灭火剂碳酸氢钠(NaHCO3)的灭火原理进行实验探究,请你参与.