题目内容
【题目】由于二氧化碳与氢氧化钠反应无明显现象,对此同学们展开了探究,请你参与.
【提出问题】二氧化碳与氢氧化钠能否发生反应?
【查阅资料】常温下,氢氧化钠、碳酸钠在乙醇中的溶解性如下.
溶剂 | 乙醇 | |
溶质 | 氢氧化钠 | 碳酸钠 |
溶解性 | 易溶 | 难溶 |
【方案设计】小明同学设计了如图所示装置进行探究。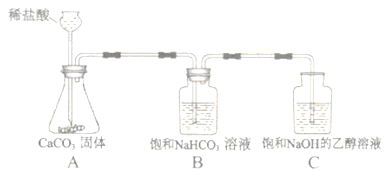
【实验探究】
(1)溶液配制.甲溶液:将一定质量的氢氧化钠固体加入到一定体积的乙醇中,用玻璃棒不断搅拌,使其成为饱和氢氧化钠的乙醇溶液.量取一定体积的乙醇要用到的仪器是 ,用玻璃棒搅拌的目的是 。
乙溶液:将一定质量的氢氧化钠固体加入到一定体积的75%的乙醇溶液中,用玻璃棒不断搅拌,使其成为不饱和氢氧化钠的乙醇溶液.判断甲、乙溶液形成的现象是 。
(2)进行实验,按图所示装置加入药品后进行实验.A中发生反应的化学方程式为 ,B装置的作用是 ,C中观察到的现象是 。
【实验结论】
(3)由此小明得出二氧化碳与氢氧化钠发生了化学反应,反应的化学方程式为 。
【反思交流】
(4)小刚同学认为小明的实验还足以证明二氧化碳与氢氧化钠发生了化学反应,还应补充的实验是 。
(5)若将图C中甲溶液换成乙溶液进行实验,C中可能无明显现象发生,原因可能是 。
【答案】(1)量筒和胶头滴管;加速溶解
(2)2HCl+CaCO3=CaCl2+H2O+CO2 ↑;除去氯化氢;溶液变浑浊
(3)2NaOH+CO2=Na2CO3+H2O
(4)将二氧化碳通入乙醇溶液,观察现象(5)碳酸钠易溶于水
【解析】
试题分析:量取一定体积的乙醇,因为乙醇是液体所以要用到的仪器是量筒和胶头滴管;用玻璃棒搅拌的目的是加速溶解,因为甲是饱和溶液而乙是不饱和溶液所以判断甲、乙溶液形成的现象是甲烧杯底部有固体,乙烧杯底部没有固体;A中发生反应的化学方程式为2HCl+CaCO3=CaCl2+H2O+CO2 ↑;B装置的作用是除去氯化氢气体;氢氧化钠和二氧化碳生成碳酸钠,碳酸钠难溶于乙醇,所以C中观察到的现象是溶液变浑浊,二氧化碳与氢氧化钠发生了化学反应,反应的化学方程式为2NaOH+CO2=Na2CO3+H2O;小明的实验还足以证明二氧化碳与氢氧化钠发生了化学反应,还应补充的实验是将二氧化碳通入乙醇溶液,观察现象,防止是二者发生反应产生沉淀;将图C中甲溶液换成乙溶液进行实验,C中可能无明显现象发生,原因可能是碳酸钠易溶于水中,因为75%的乙醇溶液中含有水。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案【题目】人类的第二杀手﹣﹣心脑血管疾病,这类疾病患者大多数属于酸性体质,应经常食用碱性食品.根据下表的信息,这类患者应经常食用的食物为( )
食物 | 葡萄 | 牛奶 | 豆制品 | 苹果 |
pH | 3.5~4.5 | 6.3~7.3 | 7.4~7.9 | 2.9~3.3 |
A.牛奶 B.葡萄 C.苹果 D.豆制品