题目内容
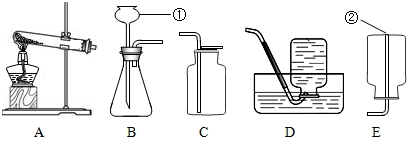
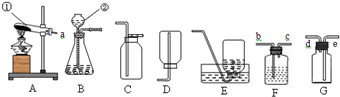
实验室制取气体的装置如图所示,根据所学的知识回答下列问题.

(1)图中标有①、②的仪器名称:①______;②______.
(2)写出用装置A和C制取氧气的一个化学方程式______.验满的方法是______.如果用如图D所示装置收集氧气,则导致所收集到的氧气不纯净的原因可能是______.如果用如图F所示装置收集氧气,气体应该从______(填“a”或“b”)端导入.
(3)可用B装置制取一种气体的化学方程式是______.用该装置还可以制取的气体是______,所选用的药品是______和______.
(4)常温下,硫化氢(H2S)是一种有臭鸡蛋气味的气体,实验室可用硫化亚铁(FeS)固体和稀硫酸反应制得,该反应方程式为FeS+H2SO4(稀)=H2S↑+FeSO4,则应选择 的发生装置为______(填序号,下同).NO气体难溶于水,密度略大于空气,易与氧气反应生成NO2,则应选择______装置来收集NO.
解:(1)①颈比较长的漏斗(不带开关)属于长颈漏斗;②收集气体的仪器是集气瓶;
(2)用装置A和C制取氧气,由图示可知是需要加热,即反应物属于固体,由于试管口没有棉花团,不能用高锰酸钾制取氧气,可以用氯酸钾和二氧化锰制取氧气,用氯酸钾和二氧化锰制取氧气,反应物是氯酸钾,生成物是氯化钾和氧气,反应条件是二氧化锰做催化剂加热,用最小公倍数法配平即可;由于氧气具有助燃性,能使带火星的木条复燃,所以将带火星的木条放在集气瓶口,如果复燃说明已经收集满;由于在制取气体的试管内存在空气,在收集气体时必须待气泡连续均匀冒出后,才能进行收集,否则收集到的气体中会混有空气;由于氧气的密度比空气小,如果气体从b端进入,氧气会迅速向上运动,从a端跑掉而收集不到气体,所以气体从a端进入;
(3)B装置不需要加热,所以反应物是固体和液体,制取二氧化碳的反应物是碳酸钙和盐酸不需要加热,所以可以制取二氧化碳,实验室制取CO2的反应物是碳酸钙与稀盐酸,生成物是氯化钙、水、二氧化碳,通过观察法配平即可,二氧化碳后面标上上升符号;由于用过氧化氢溶液和二氧化锰也可以制取氧气,不需要加热,所以该装置可以用来制取氧气;
(4)根据反应方程式为FeS+H2SO4(稀)=H2S↑+FeSO4,可知反应条件不需要加热,所以发生装置选择B;NO气体难溶于水,可以用排水法收集,密度略大于空气,易与氧气反应生成NO2,不能用排空气法收集,否则会因为变质而收集不到一氧化氮气体.
故答案为:(1)①长颈漏斗;②集气瓶;(2)2KClO3 2KCl+3O2↑;将带火星的木条放在集气瓶口,如果复燃说明已经收集满;没待气泡连续均匀冒出就进行收集;a;(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;氧气;过氧化氢溶液;二氧化锰;(4)B;D.
2KCl+3O2↑;将带火星的木条放在集气瓶口,如果复燃说明已经收集满;没待气泡连续均匀冒出就进行收集;a;(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;氧气;过氧化氢溶液;二氧化锰;(4)B;D.
分析:(1)熟记常见仪器的名称和用途;(2)根据方程式的书写方法写出反应原理,根据氧气的性质确定验满方法;根据导致收集到不纯气体的过程,考虑收集到不纯气体的原因;根据氧气的密度与水的密度的比较考虑进气口;(3)根据发生装置的特点推出制取气体的反应物的状态,结合方程式的书写回答本题;(4)根据反应方程式的反应条件考虑发生装置的选择,根据一氧化氮的溶解性、密度与空气中成分是否反应,考虑一氧化氮的收集方法.
点评:本题容易出错的地方是导致所收集到的氧气不纯净的原因,可能是由于试管内开始存在空气,没待气泡连续均匀冒出就进行了收集,或者是由于集气瓶内没装满水而进入空气.
(2)用装置A和C制取氧气,由图示可知是需要加热,即反应物属于固体,由于试管口没有棉花团,不能用高锰酸钾制取氧气,可以用氯酸钾和二氧化锰制取氧气,用氯酸钾和二氧化锰制取氧气,反应物是氯酸钾,生成物是氯化钾和氧气,反应条件是二氧化锰做催化剂加热,用最小公倍数法配平即可;由于氧气具有助燃性,能使带火星的木条复燃,所以将带火星的木条放在集气瓶口,如果复燃说明已经收集满;由于在制取气体的试管内存在空气,在收集气体时必须待气泡连续均匀冒出后,才能进行收集,否则收集到的气体中会混有空气;由于氧气的密度比空气小,如果气体从b端进入,氧气会迅速向上运动,从a端跑掉而收集不到气体,所以气体从a端进入;
(3)B装置不需要加热,所以反应物是固体和液体,制取二氧化碳的反应物是碳酸钙和盐酸不需要加热,所以可以制取二氧化碳,实验室制取CO2的反应物是碳酸钙与稀盐酸,生成物是氯化钙、水、二氧化碳,通过观察法配平即可,二氧化碳后面标上上升符号;由于用过氧化氢溶液和二氧化锰也可以制取氧气,不需要加热,所以该装置可以用来制取氧气;
(4)根据反应方程式为FeS+H2SO4(稀)=H2S↑+FeSO4,可知反应条件不需要加热,所以发生装置选择B;NO气体难溶于水,可以用排水法收集,密度略大于空气,易与氧气反应生成NO2,不能用排空气法收集,否则会因为变质而收集不到一氧化氮气体.
故答案为:(1)①长颈漏斗;②集气瓶;(2)2KClO3
 2KCl+3O2↑;将带火星的木条放在集气瓶口,如果复燃说明已经收集满;没待气泡连续均匀冒出就进行收集;a;(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;氧气;过氧化氢溶液;二氧化锰;(4)B;D.
2KCl+3O2↑;将带火星的木条放在集气瓶口,如果复燃说明已经收集满;没待气泡连续均匀冒出就进行收集;a;(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;氧气;过氧化氢溶液;二氧化锰;(4)B;D.分析:(1)熟记常见仪器的名称和用途;(2)根据方程式的书写方法写出反应原理,根据氧气的性质确定验满方法;根据导致收集到不纯气体的过程,考虑收集到不纯气体的原因;根据氧气的密度与水的密度的比较考虑进气口;(3)根据发生装置的特点推出制取气体的反应物的状态,结合方程式的书写回答本题;(4)根据反应方程式的反应条件考虑发生装置的选择,根据一氧化氮的溶解性、密度与空气中成分是否反应,考虑一氧化氮的收集方法.
点评:本题容易出错的地方是导致所收集到的氧气不纯净的原因,可能是由于试管内开始存在空气,没待气泡连续均匀冒出就进行了收集,或者是由于集气瓶内没装满水而进入空气.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目