题目内容
【题目】同学们在学习酸碱的化学性质时构建了如图知识网络,A、B、C、D是不同类别的无机化合物,“-”表示物质在一定条件下可以发生化学反应。请回答下列问题:
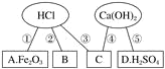
(1)反应①的化学方程式为____________________________________________________;反应的实验现象有___________________________________________。
(2)物质C应是酸、碱、盐中的哪类物质?________。
(3)写出图中一个中和反应的化学方程式________________________________________。
【答案】(1)Fe2O3 + 6HCl= 2FeCl3 + 3H2O ;红色固体逐渐溶解,溶液由无色变成黄色 ;
(2)盐
(3)Ca(OH)2 + H2SO4=CaSO4+ 2H2O
【解析】
试题(1)氧化铁是红色(或红棕色)的金属氧化物,能和盐酸反应生成氯化铁和水,即Fe2O3+6HCl=2FeCl3+3H2O,现象是:红色(或红棕色)固体不断溶解,溶液由无色变成黄色,故答案为:Fe2O3+6HCl=2FeCl3+3H2O;红色(或红棕色)固体不断溶解,溶液由无色变成黄色;(2)根据图示可以看出C既可以和盐酸反应又可以和氢氧化钙反应,应该是一种(可溶性)盐,故答案为:(可溶性)盐;(3)中和反应是酸和碱之间反应生成盐和水的反应,氢氧化钙是强碱,盐酸是强酸,二者之间可以发生中和反应,故答案为:Ca(OH)2+2HCl=CaCl2+2H2O (或HCl和任意一种碱);

 名校课堂系列答案
名校课堂系列答案【题目】从A或B中任选一个作答。若均作答,按A计分。
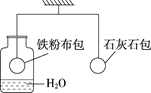
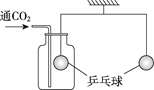
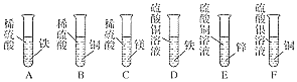
利用下图所示的装置完成实验(杠杆已经调至平衡)。
A | B |
放置较长一段时间后,左边铁粉布包______(填“上升”或“下降”),是因为铁粉与________发生了反应。 | 通入二氧化碳一段时间,左边乒乓球____(填“上升”或“下降”),再向集气瓶中滴入足量NaOH溶液,杠杆逐渐趋于平衡,发生反应的化学方程式为________。 |
|
|