题目内容
【题目】金属及其制品是现代生活中常见的材料,请回答下列问题:
(1)铁和铝都可以制作炊具,主要利用了它们的_____(填“导电”或“导热”)性.
(2)在空气中_____(填“铝”或“铁”)制品更耐腐蚀.
(3)工业上制金属钛(Ti)是在高温下,用镁与TiCl4发生置换反应而得到钛,写出该反应的化学方程式_______.
(4)向氯化铜和氯化镁混合溶液中加入一定量的锌粉,待充分反应后过滤,向滤渣中滴加稀盐酸,有气体产生,则滤渣中一定含有_____(填化学式),滤液中一定含有的溶质为____(填化学式).
(5)小明用6.5g可能含有铜、铝、镁中的一种或几种杂质的锌粉样品,跟足量的稀盐酸完全反应,生成0.2g氢气,则此锌粉样品中一定含有的杂质是_____.
(6)用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是_____t(计算结果保留到0.1).
【答案】导热 铝 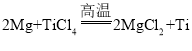 Zn、Cu ZnCl2、MgCl2 铜 583.3
Zn、Cu ZnCl2、MgCl2 铜 583.3
【解析】
(1)铁和铝都可以制作炊具,主要利用了它们的导热性,故填:导热;
(2)铝的化学性质比较活泼,在常温下,能与空气中的氧气反应,在其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化,所以在空气中铝制品更耐腐蚀,故填:铝;
(3)四氯化钛和镁在高温的条件下反应生成氯化镁和钛,该反应的化学方程式为: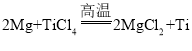 ;
;
(4)金属活动顺序表中,前边的金属可以把后边的金属从其盐溶液中置换出来,所以向氯化铜和氯化镁混合溶液中,加入一定量的锌粉,锌会和氯化铜溶液反应生成氯化锌和铜,待充分反应后过滤,向滤渣中滴加稀盐酸,有气体产生,说明有排在氢前面的锌的存在,说明锌过量,所以留在滤纸上的物质有铜,但是锌不能和氯化镁反应,所以没有镁,因此滤渣一定含有锌和铜;溶质一定含有反应生成的氯化锌及没有反应的氯化镁;故填:Zn、Cu;ZnCl2、MgCl2;
(5)假设这6.5g全部为锌,设生成氢气质量为x
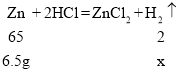
![]()
x=0.2g
依据金属与酸反应时生成的氢气质量=![]() ×金属的质量可得,假设6.5g是铝、镁或铁则生成氢气质量都大于0.2g,所以必须含有产生氢气小于0.2g的金属,在这几种金属中只有铜不与酸反应,所以此锌粉中一定含有的金属杂质是铜,故填:铜。
×金属的质量可得,假设6.5g是铝、镁或铁则生成氢气质量都大于0.2g,所以必须含有产生氢气小于0.2g的金属,在这几种金属中只有铜不与酸反应,所以此锌粉中一定含有的金属杂质是铜,故填:铜。
(6)解:设理论上可以炼出含铁96%的生铁的质量为x
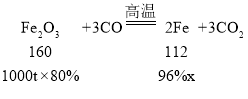
![]()
x≈583.3t
答:理论上可以炼出含铁96%的生铁的质量为583.3t。

 华东师大版一课一练系列答案
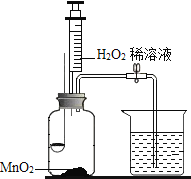
华东师大版一课一练系列答案【题目】用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验。已知:白磷的着火点为40℃。
内容步骤 | (实验1)研究燃烧条件 | (实验2)研究氧气性质 |
Ⅰ | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞 | 烧杯中盛有NaOH溶液(能吸收CO2),燃烧匙中放入木炭 点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
Ⅱ | 推入适量H2O2溶液 | 推入适量H2O2溶液 |
(1)H2O2稀溶液与MnO2接触时发生反应的化学方程式为____________________。
(2)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是________、_________;推入H2O2溶液打开止水夹,观察到烧杯中的现象是_________。
(3)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是__________;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶。该实验中,集气瓶内压强的变化过程是___________。
(4)下面是一些常用的灭火方法的事例:
①熄灭酒精灯时,用灯帽盖灭;②熄灭燃气灶火焰时,关闭阀门;③油锅着火时,用锅盖盖灭;④森林着火时,将大火蔓延线路前的一片树木砍掉;⑤房屋着火时,用高压水枪灭火。请你从灭火原理角度,选择一种分类标准进行分类:分类标准________,包括事例_________(填序号)。