题目内容
【题目】化学与生活息息相关一一“学习道路千万条,学好化学第一条”。
(1)铜和石墨都具有良好的_____性,可作导电材料。
(2)利用洗洁精具有_____功能, 能洗去餐具上的油污。
(3)保险丝(铅锑合金)比组成它的纯金属的熔点_____ ( “高”或“低”)。
(4)喝下汽水后会打嗝,原因是_____。
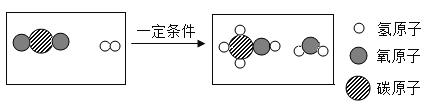
(5)由生铁炼钢时,硅与氧化亚铁在高温条件下反应生成二氧化硅和铁,写出该反应的化学方程式:_____。
【答案】导电 乳化 低 人体内温度比汽水在外界的温度高,喝下汽水后温度升高,二氧化碳的溶解度降低,多余的二氧化碳以打嗝的形式排出体外 ![]()
【解析】
(1)铜和石墨都具有良好的导电性,可作导电材料。
(2)利用洗洁精具有乳化功能, 能洗去餐具上的油污。
(3)合金的熔点比成分金属的熔点低,则保险丝(铅锑合金)比组成它的纯金属的熔点低。
(4)汽水中溶解的有二氧化碳,气体的溶解度随着温度的升高而减小,喝下汽水后会打嗝,原因是人体内的温度比汽水在外界的温度更高,使得二氧化碳的溶解度降低,多余的二氧化碳就以打嗝的方式排除体外。
(5)由生铁炼钢时,硅与氧化亚铁在高温条件下反应生成二氧化硅和铁,该反应的化学方程式为![]() 。
。

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案【题目】某些铜制品在空气中久置,表面生成绿色的铜锈(又称铜绿)。某化学实验小组设计并进行实验,探究铜生锈的条件和铜锈的成分。
[提出猜想]根据空气的成分推测,铜生锈可能与CO2、H2O和O2有关。
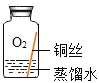
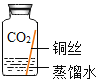
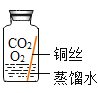
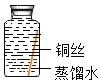
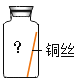
[进行实验]实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
现象 | 无明显现象 | 无明显现象 | 铜丝表而有绿色物质 | 无明显现象 | 无明显现象 |
[解释与结论]
(1)猜想与假设时,同学们认为铜生锈与N2无关,其理由是_____________。
(2)依据___________(填序号)两个实验可以得出“铜生锈一定与O2有关”的结论。
(3)为验证猜想,图中实验⑤中应选取的物质是________________。
(4)由上述实验可推知,铜生锈的条件是_______________。
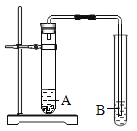
(5)同学们用如图所示装置检验出铜制品表面的绿色物质中含有碳酸盐,则A 中的溶液是_____________,现象为_________________,B中的现象为________________。
【题目】为探究盐酸的化学性质,某化学小组做了如下实验:
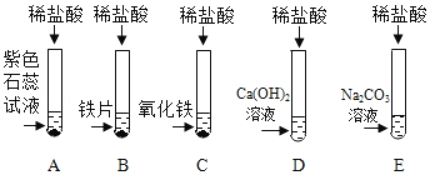
(1)A试管中的实验现象为_____,C试管中所发生反应的化学方程式为_____。
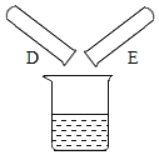
(2)将反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
(提出问题)滤液中溶质的成分是什么?
(作出猜想)猜想:NaCl
猜想二:NaCl和CaCl2
猜想三:_____
猜想四:NaCl、Ca(OH)2和HCl
(进行讨论)经过讨论,同学们一致认为猜想_____是错误的。
(设计实验)请完成实验报告。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量的碳酸钠溶液。 | _____ | 猜想二不成立 |
取少量滤液于试管中,滴加_____(填名称)。 | _____ | 猜想三成立 |
(迁移拓展)稀盐酸、稀硫酸有一些相似的化学性质,是因为在不同的酸溶液中都含有_____。
【题目】已知复分解反应![]() 可进行。在常温下,测得相同浓度的下列六种溶液的pH:表中数据揭示出复分解反应的一条规律,即碱性较强的物质发生类似反应可以生成碱性弱的物质。依照该规律,请你判断下列反应不能成立的是
可进行。在常温下,测得相同浓度的下列六种溶液的pH:表中数据揭示出复分解反应的一条规律,即碱性较强的物质发生类似反应可以生成碱性弱的物质。依照该规律,请你判断下列反应不能成立的是
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 8.6 | 11.6 | 10.3 | 11.1 |
A.![]()
B.![]()
C.![]()
D.![]()