题目内容
【题目】下列是初中的常见实验,下列说法不正确的是( )
A. 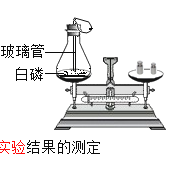
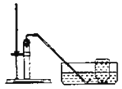
该实验中,白磷不足也不影响实验结果的测定
B. 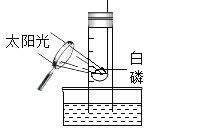
利用该装置测定空气中氧气的含量,若玻璃管内水面上升低于管内体积![]() ,可能是白磷不足引起的
,可能是白磷不足引起的
C. 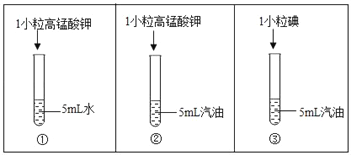
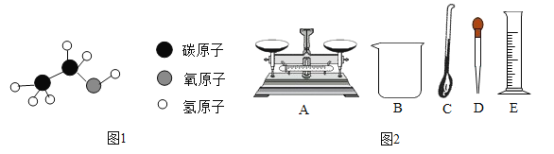
对比实验①、②可得出不同溶质在同一溶剂中溶解性不相同。
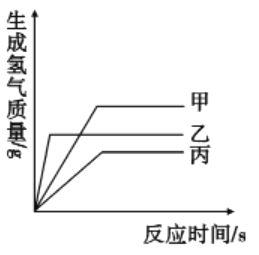
D. 
点燃负极的气体,发出淡蓝色火焰,烧杯壁有水珠出现,可见,通过分解水和合成水都可以探究水的组成
【答案】C
【解析】
A、白磷与氧气在点燃的条件下反应生成五氧化二磷,参加反应的白磷与氧气的质量之和等于生成的五氧化二磷的质量,即使白磷的量不足反应后天平依然平衡,不影响实验结果的测定,故选项正确;
B、利用图示装置测定空气中氧气的含量时,若白磷的量不足、装置漏气或装置没有冷却至室温就读数均会造成测定结果偏小,故选项正确;
C、实验1是1小粒高锰酸钾放入5mL水中,实验2是1小粒高锰酸钾放入5mL汽油中,这两组实验对比探究了同种溶质在不同溶剂中的溶解性不同,故选项不正确;
D、通电分解水生成氢气和氧气;氢气与氧气在点燃的条件下反应生成水,由质量守恒定律可知,两个实验均能证明水是由氢元素与氧元素组成的,故选项正确。故选C。

【题目】为探究锌、铜、铬三种金属的性质,某兴趣小组进行如下实验。
【实验一】将三种金属丝分别与一节干电池和小电珠连接,小电珠发光。
【实验二】取粗细、长短相同的锌丝、铜丝、铬丝均与50mL稀硫酸反应,实验记录如下:
锌 | 铜 | 铬 | 铜 | |
稀硫酸的质量分数 | 5% | 5% | 15% | 15% |
反应现象 | 少量气泡 | 无现象 | 许多气泡 | 无现象 |
【实验三】金属锌、铜和稀硫酸构成如图所示的化学电池装置,观察到铜片表面有气泡(H2),小电珠发光。

(1)实验一的现象说明三种金属都具有____________性;
(2)铬与稀硫酸反应生成硫酸亚铬(CrSO4)和氢气,反应的化学方程式是______________________________________;该反应属于________________(填基本反应类型)反应;
(3)要判断三种金属活动性强弱,必须在实验二的基础上增补一个实验才能得出结论,其实验内容是把粗细、长短相同的________________放入________________的50mL稀硫酸中,观察放出气泡的快慢;
(4)金属活动性强弱是由金属物质的结构决定的,不会因某个实验而改变。下列关于实验三分析正确的是______(填序号)。
A.铜的金属活动性变得比锌强
B.铜与稀盐酸发生了置换反应
C.该装置将化学能转化为电能
【题目】小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种叫做过氧化钙的淡黄色固体,用来增加鱼池中的含氧量。小明刚学完氯气的实验室制法,于是他想可否用过氧化钙在实验室制取氧气。
(提出问题)过氧化钙可否用于制取氧气?
(查阅资料)部分内容如下:过氧化钙![]() 室温下稳定,在
室温下稳定,在![]() 时分解成氧气,放入水中可与水反应放出氧气,常用作鱼池增氧剂、杀菌剂等。
时分解成氧气,放入水中可与水反应放出氧气,常用作鱼池增氧剂、杀菌剂等。
![]() 小明提出猜想I:加热过氧化钙可制取氧气。
小明提出猜想I:加热过氧化钙可制取氧气。
实验装置 | 实验主要过程 |
|
|
实验结论:实验室中可加热过氧化钙制取氧气。
![]() 小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ过氧化钙与水
小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ过氧化钙与水
反应可制取氧气。
实验装置 | 实验主要过程 |
|
|
实验结论:实验室______![]() 填能或不能
填能或不能![]() 用过氧化钙与本反应制取氧气。
用过氧化钙与本反应制取氧气。
分析与反思:
![]() 虽然没有快速收集到大量氧气;但由此实验现象,小明认为鱼池用过氧化钙做鱼池增氧剂的主要原因是______。
虽然没有快速收集到大量氧气;但由此实验现象,小明认为鱼池用过氧化钙做鱼池增氧剂的主要原因是______。
![]() 小明希望对此实验进行改进,使该反应速率加快,你能帮他提出建议吗?
小明希望对此实验进行改进,使该反应速率加快,你能帮他提出建议吗?
你的合理建议是:______。
以上建议是否可行,还需进一步通过实验验证。