题目内容
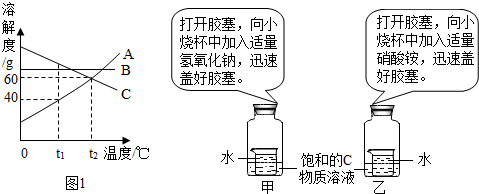
图1是A、B、C三种物质的溶解度曲线.请回答:

(1)t1℃时,A、B、C三种物质的溶解度由小到大的顺序是______.
(3)t1℃时,向100g水中加入70gA物质,然后升温至t2℃,此时得到的溶液的质量是______.
(2)使物质B从溶液中结晶析出的最佳方法是______.
(4)根据溶解度曲线图及下图所示回答问题:可观察到甲乙两瓶中有固体析出的是______(填“甲”或“乙”),原因是______.
解:(1)t1℃时,A、B、C三种物质的溶解度由小到大的顺序是 C>B>A;
(3)t1℃时A 的溶解度是40g,向100g水中加入70gA物质最多溶解40g,然后升温至t2℃,此时溶解度变为60g,得到的溶液的质量是160g;
(2)B的溶解度随温度的变化不大,所以要使B从溶液中结晶析出,最好采用蒸发溶剂的方法;
(4)C的溶解度随温度升高而减小,所以甲、乙两瓶中要有固体析出,则须使溶液温度升高,而氢氧化钠固体溶于水放热,硝酸铵溶于水吸热,故甲瓶中有固体析出;
故答案为:(1)C>B>A;(2)160g;(3)蒸发溶剂;(4)甲;氢氧化钠固体溶于水放热,使溶液的温度升高,C的溶解度随温度的升高而减小,故会析出固体.
分析:(1)据溶解度曲线可比较同一温度下不同物质的溶解度;
(2)据t2℃时A的溶解度分析判断;
(3)B的溶解度随温度的变化不大,所以要使B从溶液中结晶析出,最好采用蒸发溶剂的方法;
(4)C的溶解度随温度升高而减小,所以甲、乙两瓶中要有固体析出,则须使溶液温度升高.
点评:了解溶解度曲线的意义及应用,能较好考查学生分析、解决问题的能力.
(3)t1℃时A 的溶解度是40g,向100g水中加入70gA物质最多溶解40g,然后升温至t2℃,此时溶解度变为60g,得到的溶液的质量是160g;
(2)B的溶解度随温度的变化不大,所以要使B从溶液中结晶析出,最好采用蒸发溶剂的方法;
(4)C的溶解度随温度升高而减小,所以甲、乙两瓶中要有固体析出,则须使溶液温度升高,而氢氧化钠固体溶于水放热,硝酸铵溶于水吸热,故甲瓶中有固体析出;
故答案为:(1)C>B>A;(2)160g;(3)蒸发溶剂;(4)甲;氢氧化钠固体溶于水放热,使溶液的温度升高,C的溶解度随温度的升高而减小,故会析出固体.
分析:(1)据溶解度曲线可比较同一温度下不同物质的溶解度;
(2)据t2℃时A的溶解度分析判断;
(3)B的溶解度随温度的变化不大,所以要使B从溶液中结晶析出,最好采用蒸发溶剂的方法;
(4)C的溶解度随温度升高而减小,所以甲、乙两瓶中要有固体析出,则须使溶液温度升高.
点评:了解溶解度曲线的意义及应用,能较好考查学生分析、解决问题的能力.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目


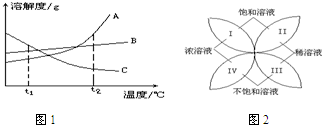 (1)请你各举出一个实例,说明下列有关溶液的叙述是错误的.
(1)请你各举出一个实例,说明下列有关溶液的叙述是错误的. 图1是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题:
图1是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题: