题目内容
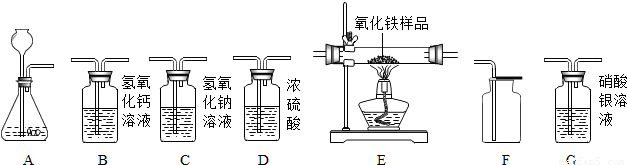
如图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器.试根据题目要求,回答下列问题:
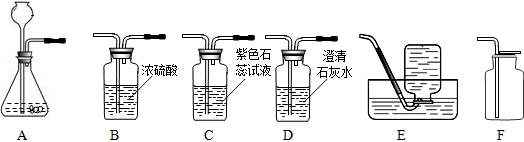
(1)甲同学将装置A-B-E连接,你认为他想制取并收集的气体是
(2)乙同学以石灰石和稀盐酸为原料在A装置中制取二氧化碳并探究二氧化碳的性质:
①生成二氧化碳时,所发生反应的化学方程式为
②若要检验制备的气体是二氧化碳,应将A与
③将产生的二氧化碳通入
④乙同学用塑料矿泉水瓶收集了一瓶二氧化碳,向瓶中迅速倒入氢氧化钠溶液后振荡,发现瓶子变瘪,于是他认为二氧化碳能与氢氧化钠反应.而甲同学认为乙同学得出的结论太草率,因为

(1)甲同学将装置A-B-E连接,你认为他想制取并收集的气体是
氧气
氧气
(氧气或二氧化碳),其中仪器B的作用是干燥作用
干燥作用
.(2)乙同学以石灰石和稀盐酸为原料在A装置中制取二氧化碳并探究二氧化碳的性质:
①生成二氧化碳时,所发生反应的化学方程式为
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.②若要检验制备的气体是二氧化碳,应将A与
D
D
(填写仪器序号字母)相连,现象是澄清的石灰水变浑浊
澄清的石灰水变浑浊
.③将产生的二氧化碳通入
C
C
中(填序号),可测定二氧化碳水溶液的酸碱性.④乙同学用塑料矿泉水瓶收集了一瓶二氧化碳,向瓶中迅速倒入氢氧化钠溶液后振荡,发现瓶子变瘪,于是他认为二氧化碳能与氢氧化钠反应.而甲同学认为乙同学得出的结论太草率,因为
二氧化碳能溶于水并与水反应
二氧化碳能溶于水并与水反应
.甲同学将瓶中的液体倒出,滴入Ca(OH)2溶液
Ca(OH)2溶液
(从酚酞试液、稀盐酸、Ca(OH)2溶液中选择其一),若看到生成白色沉淀
生成白色沉淀
现象,则证明氢氧化钠能与二氧化碳发生反应.写出与之对应的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
.分析:甲同学将装置A-B-E连接,他想制取并收集的气体是氧气,因为用过氧化氢和二氧化锰制氧气不需要加热,并且氧气不易溶于水,能用排水法收集,二氧化碳能溶于水,不能用排水法收集;浓硫酸具有吸水性,起干燥作用;制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳用澄清的石灰水检验,能使澄清的石灰水变浑浊;二氧化碳和水反应生成碳酸,因此紫色的石蕊试液变红色;甲同学认为乙同学得出的结论太草率,因为二氧化碳能溶于水并与水反应;甲同学将瓶中的液体倒出,滴入Ca(OH)2溶液,如果生成白色沉淀,则证明氢氧化钠能与二氧化碳发生反应.
解答:解:(1)甲同学将装置A-B-E连接,他想制取并收集的气体是氧气,因为用过氧化氢和二氧化锰制氧气不需要加热,并且氧气不易溶于水,能用排水法收集,二氧化碳能溶于水,不能用排水法收集;浓硫酸具有吸水性,起干燥作用;故答案为:氧气;干燥作用;
(2)实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳用澄清的石灰水检验,能使澄清的石灰水变浑浊;二氧化碳和水反应生成碳酸,因此紫色的石蕊试液变红色;甲同学认为乙同学得出的结论太草率,因为二氧化碳能溶于水并与水反应;甲同学将瓶中的液体倒出,滴入Ca(OH)2溶液,如果生成白色沉淀,则证明氢氧化钠能与二氧化碳发生反应,因为碳酸钠和氢氧化钙反应生成碳酸钙和水;故答案为:①CaCO3+2HCl=CaCl2+H2O+CO2↑;②D;澄清的石灰水变浑浊;③C;④二氧化碳能溶于水并与水反应;Ca(OH)2;生成白色沉淀;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(2)实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳用澄清的石灰水检验,能使澄清的石灰水变浑浊;二氧化碳和水反应生成碳酸,因此紫色的石蕊试液变红色;甲同学认为乙同学得出的结论太草率,因为二氧化碳能溶于水并与水反应;甲同学将瓶中的液体倒出,滴入Ca(OH)2溶液,如果生成白色沉淀,则证明氢氧化钠能与二氧化碳发生反应,因为碳酸钠和氢氧化钙反应生成碳酸钙和水;故答案为:①CaCO3+2HCl=CaCl2+H2O+CO2↑;②D;澄清的石灰水变浑浊;③C;④二氧化碳能溶于水并与水反应;Ca(OH)2;生成白色沉淀;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的检验等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
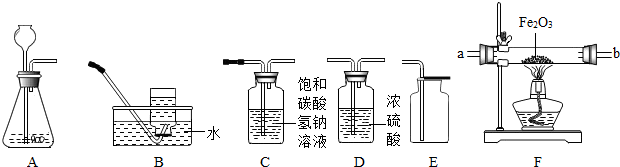
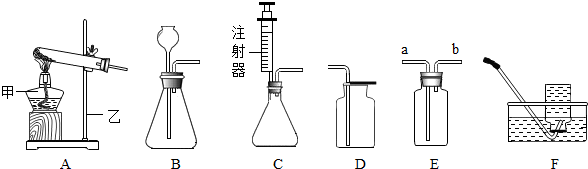

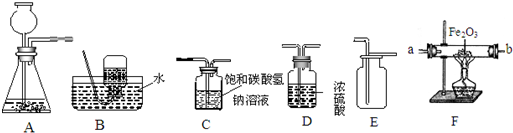
 2Fe+3CO2)
2Fe+3CO2)