题目内容
(2012?槐荫区二模)如图所示为实验室中常见气体的制备、干燥、收集和性质实验的部分仪器.试根据题目要求,回答下列问题:(设过程中所有发生的反应都恰好完全进行).
(1)若以石灰石和稀盐酸(盐酸有挥发性)为原料制取二氧化碳气体,现要制备并收集一瓶干燥、纯净的二氧化碳气体.
①所选仪器的连接顺序为
②生成二氧化碳的化学方程式为:
③要除去二氧化碳气体中混有的氯化氢气体,请从NaOH溶液、水、AgNO3溶液中选择一种,并简述理由
(2)实验室制得的一氧化碳中常混有二氧化碳和水蒸气,欲用纯净、干燥的一氧化碳还原氧化铁并检验生成的气体,某同学所选装置的连接顺序为:制得的一氧化碳气体→装置C→装置D→装置E→装置B.(友情提示:3CO+Fe2O3
2Fe+3CO2)
①装置C的作用是
②装置E中看到的现象是
③该实验产生的尾气会造成环境污染,请你写出处理尾气的方法

(1)若以石灰石和稀盐酸(盐酸有挥发性)为原料制取二氧化碳气体,现要制备并收集一瓶干燥、纯净的二氧化碳气体.
①所选仪器的连接顺序为
AGDF
AGDF
(填写仪器序号字母).②生成二氧化碳的化学方程式为:
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.③要除去二氧化碳气体中混有的氯化氢气体,请从NaOH溶液、水、AgNO3溶液中选择一种,并简述理由
选AgNO3溶液,因为氯化氢气体可与AgNO3溶液反应,而二氧化碳与之不反应
选AgNO3溶液,因为氯化氢气体可与AgNO3溶液反应,而二氧化碳与之不反应
.(2)实验室制得的一氧化碳中常混有二氧化碳和水蒸气,欲用纯净、干燥的一氧化碳还原氧化铁并检验生成的气体,某同学所选装置的连接顺序为:制得的一氧化碳气体→装置C→装置D→装置E→装置B.(友情提示:3CO+Fe2O3
| ||
①装置C的作用是
吸收二氧化碳(或除去二氧化碳)
吸收二氧化碳(或除去二氧化碳)
;②装置E中看到的现象是
红色粉末变为黑色
红色粉末变为黑色
.③该实验产生的尾气会造成环境污染,请你写出处理尾气的方法
在装置末端放一个酒精灯或用气球收集
在装置末端放一个酒精灯或用气球收集
.分析:(1)①实验室制取CO2,是在常温下,用大理石和盐酸反应,不需要加热.要收集一瓶干燥、纯净的二氧化碳气体,就要把杂质氯化氢气体和水蒸气除去,氯化氢气体用硝酸银溶液除去,水蒸气用浓硫酸除去;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;
②根据大理石和稀盐酸反应原理书写方程式;
③根据氯化氢气体可与AgNO3溶液反应而被除去,二氧化碳与AgNO3溶液不能发生反应进行分析;
(2)①二氧化碳可与氢氧化钠溶液反应被除去;
②一氧化碳可与红色的氧化铁反应生成黑色的铁粉;
③可利用一氧化碳的可燃性将其燃烧掉,或用气球收集起来.
②根据大理石和稀盐酸反应原理书写方程式;
③根据氯化氢气体可与AgNO3溶液反应而被除去,二氧化碳与AgNO3溶液不能发生反应进行分析;
(2)①二氧化碳可与氢氧化钠溶液反应被除去;
②一氧化碳可与红色的氧化铁反应生成黑色的铁粉;
③可利用一氧化碳的可燃性将其燃烧掉,或用气球收集起来.
解答:解:(1)①要收集一瓶干燥、纯净的二氧化碳气体,就要把杂质氯化氢气体和水蒸气除去,氯化氢气体与硝酸银溶液反应生成氯化银白色沉淀和硝酸,因此可以除去氯化氢气体,水蒸气用浓硫酸除去;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,因此仪器的连接顺序为:AGDF;
②碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
③二氧化碳与NaOH溶液、水可发生反应,所以气体若通过NaOH溶液、水,不仅除去氯化氢,而且把二氧化碳也除去了,这与实验目的是相违背的,故不可行;而氯化氢气体可与AgNO3溶液反应,且不与二氧化碳,符合条件;
(2))①通过装置C氢氧化钠溶液是为了反应掉气体中的二氧化碳;
②一氧化碳可与红色的氧化铁反应生成黑色的铁粉;
③可利用一氧化碳的可燃性将其燃烧掉,或用气球收集起来;
故答案为:
(1)①AGDF;②CaCO3+2HCl=CaCl2+H2O+CO2↑;③选AgNO3溶液,因为氯化氢气体可与AgNO3溶液反应,而二氧化碳与之不反应;
(2)①吸收二氧化碳(或除去二氧化碳);②红色粉末变为黑色;③在装置末端放一个酒精灯或用气球收集.
②碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
③二氧化碳与NaOH溶液、水可发生反应,所以气体若通过NaOH溶液、水,不仅除去氯化氢,而且把二氧化碳也除去了,这与实验目的是相违背的,故不可行;而氯化氢气体可与AgNO3溶液反应,且不与二氧化碳,符合条件;
(2))①通过装置C氢氧化钠溶液是为了反应掉气体中的二氧化碳;
②一氧化碳可与红色的氧化铁反应生成黑色的铁粉;
③可利用一氧化碳的可燃性将其燃烧掉,或用气球收集起来;
故答案为:
(1)①AGDF;②CaCO3+2HCl=CaCl2+H2O+CO2↑;③选AgNO3溶液,因为氯化氢气体可与AgNO3溶液反应,而二氧化碳与之不反应;
(2)①吸收二氧化碳(或除去二氧化碳);②红色粉末变为黑色;③在装置末端放一个酒精灯或用气球收集.
点评:熟记实验室制取二氧化碳的反应原理、注意事项以及物质的检验和除杂的知识,一氧化碳还原氧化铁实验的现象和注意事项等,要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
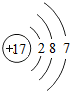 (2012?槐荫区二模)某粒子的结构示意图如图所示,下列关于该粒子的说法中,错误的是( )
(2012?槐荫区二模)某粒子的结构示意图如图所示,下列关于该粒子的说法中,错误的是( )