题目内容
【题目】10%的KNO3不饱和溶液100 g,在温度不变的条件下,欲使溶质的质量分数变为20%,下列方法中,最可行的是( )
A. 再加入12.5 g KNO3溶解完
B. 再加入10 g KNO3溶解完
C. 再加入100 g 10%的KNO3溶液
D. 恒温蒸发掉45 g水
【答案】A
【解析】
A、如果采取加溶质的方法来实现,设加入硝酸钾的质量为x,则
![]() ×100%=20%,x=12.5 g
×100%=20%,x=12.5 g
加入12.5g硝酸钾完全溶解后所得溶液的溶质质量分数为20%,故可行;
B、加入10 g硝酸钾完全溶解后所得溶液的溶质质量分数小于20%,故不可行;
C、加入10%的硝酸钾溶液,溶质质量分数仍为10%,故不可行;
D、如果采取蒸发溶剂的方法来实现,设需蒸发掉水的质量为y,则
![]() ×100%=20%,y=50 g。蒸发掉45 g水后所得溶液中溶质质量分数小于20%,故不可行。
×100%=20%,y=50 g。蒸发掉45 g水后所得溶液中溶质质量分数小于20%,故不可行。
故选A。

练习册系列答案
相关题目
【题目】t1℃时,将甲、乙、丙三种固体各20克,分别加入盛有50克水的烧杯中,充分溶解后的情况如下表
物质 | 甲 | 乙 | 丙 |
未溶解的固体/g | 5.4 | 0 | 2 |
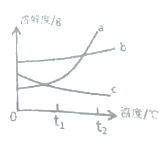
(1)一定是饱和溶液的是_______,t1℃时丙的溶解度为_______。
(2)图中表示固体甲的曲线是________。
(3)t1℃时,甲乙丙的溶解度大小关系为_______。
(4)t2℃时,取等质量的甲乙丙的饱和溶液,分别恒温蒸发等质量的水,析出溶质质量的大小关系为______(用甲乙丙表示)