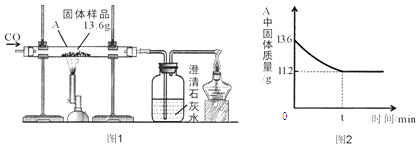
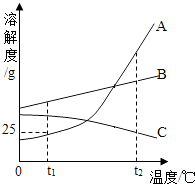
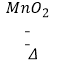题目内容
【题目】实验室想探究影响化学反应因素,设计如下方案,请完成如表,回答相关问题:
实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
实验Ⅰ | 探究温度对H2O2分解速率的影响 | 25℃ | 1g氧化铁 | 10mL 5%的H2O2溶液 |
实验Ⅱ | 45℃ | 2g二氧化锰 | 10mL 6%的H2O2溶液 |
(1)结果实验Ⅱ的反应速率更快,很多同学一致认为温度越高,过氧化氢溶液分解越快,但王老师认为他们的实验方案设计不完全正确,请你找出该实验不恰当的地方是(请说出2点)、 .
(2)若用5g二氧化锰跟氯酸钾混合加热制取9.6g的氧气,至少需要多少克的氯酸钾?反应结束后残留固体质量至少有多少?(请利用化学方程式计算,并写出解题过程)
【答案】
(1)催化剂的质量不同;过氧化氢溶液的浓度不同
(2)解:设需要氯酸钾的质量为x,生成氯化钾的质量y,
2KClO3 |
| 2KCl | + | 3O2↑ |
245 | 149 | 96 | ||
x | y | 9.6g |
![]()
x=24.5g,y=14.9g,
反应结束后残留固体质量为:5g+14.9g=19.9g,
答:若用5g二氧化锰跟氯酸钾混合加热制取9.6g的氧气,至少需要24.5g的氯酸钾,反应结束后残留固体质量至少有19.9g
【解析】解:(1)该实验不恰当的地方有:催化剂不同,催化剂的质量不同,过氧化氢热源的浓度不同,通过该实验不能得出温度越高,过氧化氢溶液分解越快的结论.
故填:催化剂的质量不同;过氧化氢溶液的浓度不同.
【考点精析】本题主要考查了催化剂的特点与催化作用和根据化学反应方程式的计算的相关知识点,需要掌握催化剂(触媒):在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质.(一变两不变)催化剂在化学反应中所起的作用叫催化作用;各物质间质量比=系数×相对分子质量之比才能正确解答此题.

练习册系列答案
相关题目