题目内容
【题目】实验室制取二氧化碳气体,并验证某些性质。
①常见物质中,碳、一氧化碳都可以和同一物质发生化合反应得到二氧化碳,该物质是________;而![]() 不能通过化合反应得到二氧化碳,理由是_____________________。利用大理石制取二氧化碳的化学方程式___________________。
不能通过化合反应得到二氧化碳,理由是_____________________。利用大理石制取二氧化碳的化学方程式___________________。
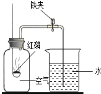
②空气中排放过多的二氧化碳会造成__________效应。为验证该效应,利用如图装置收集一瓶二氧化碳气体,应由____________(选填“长”“短”)导管通入二氧化碳,验证收集满了的方法是________。实验时,还需一瓶(同样大小)装满_________的集气瓶放在太阳下做对照实验。
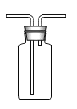
③因为二氧化碳具有______________,常用二氧化碳作灭火剂。
④如果利用足量石灰水吸收![]() 二氧化碳气体,计算所需氢氧化钙的质量为_______。(根据化学方程式列式计算)
二氧化碳气体,计算所需氢氧化钙的质量为_______。(根据化学方程式列式计算)
【答案】氧气 根据质量守恒定律的元素守恒,![]() 中含有氢元素,生成物中也会有含氢元素物质
中含有氢元素,生成物中也会有含氢元素物质 ![]() 温室 长 将一根燃着的木条放在短导管口,若木条熄灭,则收集满二氧化碳 空气 二氧化碳具有不能燃烧也不能支持燃烧,密度大于空气
温室 长 将一根燃着的木条放在短导管口,若木条熄灭,则收集满二氧化碳 空气 二氧化碳具有不能燃烧也不能支持燃烧,密度大于空气 ![]()
【解析】
①碳在氧气中燃烧生成二氧化碳,一氧化碳在氧气中燃烧生成二氧化碳。常见物质中,碳、一氧化碳都可以和同一物质发生化合反应得到二氧化碳,由于碳中不含氧元素,而二氧化碳含有氧元素,且发生的是化合反应,所以该物质是氧气;CH4不能通过化合反应得到二氧化碳,理由是甲烷中含有 H 元素,根据质量守恒定律,产物除二氧化碳外,还有含 H 元素的物质;
②空气中排放过多的二氧化碳会造成温室效应。为验证该效应,需要对比二氧化碳和空气的对比效果,利用如图装置收集一瓶二氧化碳气体,由于二氧化碳密度大于空气,所以应由长导管通入二氧化碳;二氧化碳不能燃烧也不能支持燃烧,能使燃着的木条复燃,验证收集满了的方法是将燃着的木条置于短导管口,木条熄灭则已集满实验时,还需一瓶(同样大小)装满空气的集气瓶放在太阳下做对照实验;
③因为二氧化碳具有不能燃烧也不能支持燃烧,密度大于空气,常用二氧化碳作灭火剂;
④如果利用足量石灰水吸收 0.1mol 二氧化碳气体,计算设所需氢氧化钙物质的量为x。

![]() x=0.1mol;
x=0.1mol;
氢氧化钙质量=0.1mol×74g/mol=7.4g。

 同步奥数系列答案
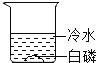
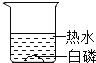
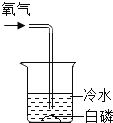
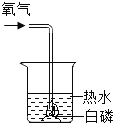
同步奥数系列答案【题目】某同学设计了如下图实验证明可燃物燃烧与氧气、温度有关。其中证明可燃物燃烧必须达到一定温度的实验是( )
编号 | 实验① | 实验② | 实验③ | 实验④ |
装 置 |
|
|
|
|
现象 | 白磷不燃烧 | 白磷不燃烧 | 白磷不燃烧 | 白磷燃烧 |
A. ①和②B. ②和③C. ②和④D. ③和④
【题目】学习小组对碱式碳酸铜[化学式为![]() ]的性质进行探究,并进行相关实验。
]的性质进行探究,并进行相关实验。
①分析组成
碱式碳酸铜中化合价为-1价的原子团是___________。
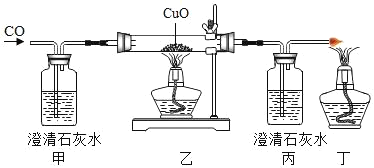
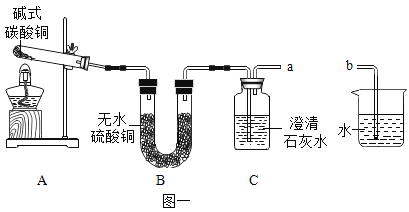
②探究分解产物,装置如图一所示(省略夹持仪器)
实验步骤 | 现象 | 分析和结论 |
Ⅰ.组装装置,连接导管a、b,微热试管。 | 烧杯中的导管口_________。 | 说明整套装置不漏气。 |
Ⅱ.加入药品和试剂,点燃酒精灯。 | A中固体出现黑色,B中白色固体变蓝,C中石灰水变浑浊。 | C中反应的化学方程式为_________。碱式碳酸铜受热分解的产物有 |
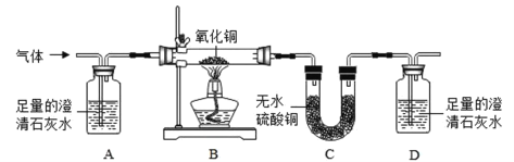
③用氢气还原装置A中反应后的固体并检验产物,装置如图二所示(F中的无水硫酸铜用于吸收空气中的水蒸气)
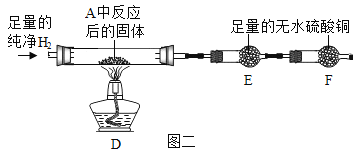
Ⅰ.D中观察到固体变红。
Ⅱ.实验开始时,若先点燃酒精灯后通氢气,可能导致的后果是______________。
Ⅲ.E中观察到白色固体变蓝,发生反应的化学方程式为______________,该现象能否证明氢气和氧化铜反应生成了水,理由是______________。
④学习小组还利用图二装置定量测定水的组成(玻璃管中为纯净氧化铜),并测定了下表的四个数据(单位:g)。
反应前质量 | 反应后质量 | |
装置D | a | b |
装置E | c | d |
利用表格中数据,列式表示水中氢、氧原子的物质的量之比______________。(不要求化简)