题目内容
【题目】金属钛(元素符号Ti)硬度大、熔点高、耐腐蚀。钛酸亚铁(FeTiO3)经过一系列反应制备钛和甲醇(CH3OH)的主要生产流程图如下:
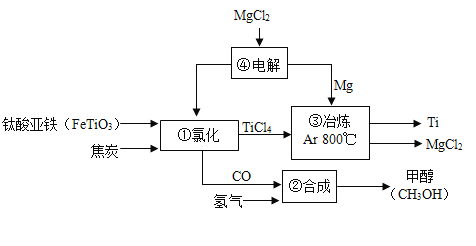
(1)①中发生反应的化学方程式为![]() ,则X的化学式为_____。
,则X的化学式为_____。
(2)③中冶炼发生反应的化学方程式为_____。该反应在氩气(Ar)中进行的理由是_____。
(3)②中为使CO全部转化为甲醇,理论上CO和H2投料的质量比为_____。
(4)绿色化学提倡物料循环利用,以上生产流程中可用于循环利用的物质有_____。
【答案】FeCl3 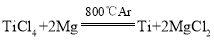 防止Mg、Ti被氧化 7:1 MgCl2
防止Mg、Ti被氧化 7:1 MgCl2
【解析】
(1)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式![]() ,反应前铁、钛、氧、碳、氯原子个数分别为2、2、6、6、14,反应后的生成物中铁、钛、氧、碳、氯原子个数分别为0、2、6、6、8,根据反应前后原子种类、数目不变,则,2X分子中含有2个铁原子和6个铁原子,则每个X分子由1个铁原子和3个氯原子构成,物质X的化学式为FeCl3;
,反应前铁、钛、氧、碳、氯原子个数分别为2、2、6、6、14,反应后的生成物中铁、钛、氧、碳、氯原子个数分别为0、2、6、6、8,根据反应前后原子种类、数目不变,则,2X分子中含有2个铁原子和6个铁原子,则每个X分子由1个铁原子和3个氯原子构成,物质X的化学式为FeCl3;
(2)根据流程图可知,反应③中冶炼发生反应是镁与TiCl4在800℃,在氩气的环境中反应生成氯化镁和钛,反应的化学方程式 ;氩气的化学性质很不活泼,该反应在氩气(Ar)中进行的理由是防止Mg、Ti被氧化.
;氩气的化学性质很不活泼,该反应在氩气(Ar)中进行的理由是防止Mg、Ti被氧化.
(3)②中反应,即一氧化碳与氢气反应生成甲醇,反应的化学方程式为CO+2H2=CH3OH,为使原料全部转化为甲醇,理论上CO和H2投料的质量比为28:(2×2)=7:1;
(4)既是反应物,也是生成物的物质,可以循环使用,以上流程中可用于循环的物质除Cl2、Mg外,还有MgCl2。

 名校课堂系列答案
名校课堂系列答案【题目】某课外兴趣小组为探究一久置的铝片中铝元素的质量分数,他们取8 g该铝片样品放入烧杯中,并依次加入一定质量的相同浓度的稀盐酸。测得相关数据如下,请回答问题。
实验次数 | 1 | 2 | 3 | 4 | 5 |
每次加入稀盐酸的质量/g | 50.0 | 100.0 | 100.0 | 100.0 | 100.0 |
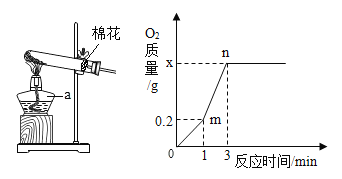
产生气体的总质量/g | 0 | 0.2 | a | 0.6 | 0.7 |
(1)a的数值为_____;
(2)列式计算所用稀盐酸的溶质质量分数_____(结果保留至0.1%)。
(3)第1次实验没有气体产生的原因可能是(用化学方程式表示)_____。
【题目】在实验室中,小希发现了一瓶敞口放置的氢氧化钙粉末试剂,猜想其成分中可能含有碳酸钙,并进行如下实验:
称取 10.0g 样品置于烧杯中,加入足量稀盐酸充分反应,烧杯及烧杯内物质总质量与反应时间的关系如下表所示:
反应时间/min | 0 | t1 | t2 | t3 |
烧杯及烧杯内物质总质量/g | 280.0 | 278.9 | 277.8 | 277.8 |
根据实验过程和实验记录提供的信息,回答下列问题:
(1)小希猜想的理由是_____(用化学方程式表示),从实验数据证实了小希的猜想成立,因此药品要_____保存.
(2)从表格中看出,反应时间_____时反应完全.
(3)计算该样品中碳酸钙的质量分数_____.