题目内容
【题目】请根据下列实验装置图,回答有关问题。
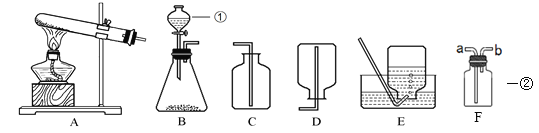
(1)写出仪器名称:①是______,②是______。
(2)若用装置B和E组合制O2,反应的化学方程式为______,该反应______(填“吸收”或“放出”)热量。若锥形瓶内反应过于剧烈,可采取的方法有______(填序号)。
①控制反应物的滴加速率 ②用小一些的锥形瓶 ③减小反应物的浓度
(3)通常状况下,甲烷密度小于空气,难溶于水。实验室常用加热无水醋酸钠和碱石灰的固体混合物来制取少量甲烷,则制取甲烷的发生装置和收集装置的组合是______。
(4)实验室制取CO2选用稀盐酸而不用浓盐酸,是因为浓盐酸具有______;制取二氧化碳的化学方程式是______,发生装置选______,收集装置选______,若要收集干燥的CO2须在发生装置和收集装置之间连接洗气装置F(如图)此时装置F内应装入______(填试剂名称),气体应从导管______(填“a”或“b”)端通入。
(5)装置F也能用来收集气体。若用排水法在其中收集氢气,应预先在瓶内______,气体应从______(填“a”或“b”)端通入。
【答案】分液漏斗 集气瓶 2H2O2![]() 2H2O+O2↑ 放出 ①③ AD或AE 挥发性 CaCO3+2HCl=CaCl2+H2O+CO2↑ B C 浓硫酸 a 装满水 b
2H2O+O2↑ 放出 ①③ AD或AE 挥发性 CaCO3+2HCl=CaCl2+H2O+CO2↑ B C 浓硫酸 a 装满水 b
【解析】
(1)据图可知仪器①是分液漏斗;②是集气瓶;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的化学方程式为:2H2O2![]() 2H2O+O2↑,本反应放热;若锥形瓶内反应过于剧烈,可采取的方法有:①控制反应物的滴加速率,③减小反应物的浓度;
2H2O+O2↑,本反应放热;若锥形瓶内反应过于剧烈,可采取的方法有:①控制反应物的滴加速率,③减小反应物的浓度;
(3)实验室常用加热无水醋酸钠和碱石灰的固体混合物来制取少量甲烷,因此需要加热,应选择装置A;通常状况下,甲烷密度小于空气,难溶于水,因此能用向下排空气法和排水法收集,应选择装置D或E;
(4)实验室制取CO2选用稀盐酸而不用浓盐酸,是因为浓盐酸具有挥发性;在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;因此不需要加热,应选择装置B;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,应选择装置C;二氧化碳可以用浓硫酸干燥,二氧化碳气体应从F装置的长管进入;
(5)装置F也能用来收集气体,若用排水法在其中收集氢气,应预先在瓶内装满水;气体应从短管进入,因为氢气的密度比水小。

 名校课堂系列答案
名校课堂系列答案【题目】下列实验设计不能达到实验目的的是( )
选项 | A | B | C | D |
实验 设计 |
|
|
|
|
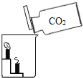
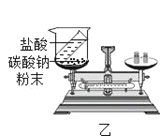
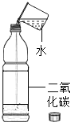
实验 目的 | 证明 CO2 比空 气的密度大 | 探究质量守恒定律 | 验证 CO2 能溶于水 | 证明石墨具有导电 性 |
A. A B. B C. C D. D