题目内容
【题目】为了从硝酸亚铁和硝酸银的混合溶液中,提取并回收银,小燕设计了如下的实验方案:
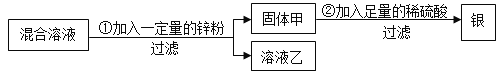
(1)若溶液乙为无色溶液,则固体甲一定含有的物质是_____,可能含有的物质是_____,写出一个在步骤①中肯定发生的反应的化学方程式_____。
(2)若溶液乙为浅绿色溶液,则溶液乙中溶质的组成可能是_____或_____(填物质的名称或化学式)。
【答案】铁、银 锌 Zn+Fe(NO3)2═Zn(NO3)2+Fe(或Zn+2AgNO3═Zn(NO3)2+2Ag) Zn(NO3)2、Fe(NO3)2 Zn(NO3)2、Fe(NO3)2、AgNO3
【解析】
(1)在金属活动性顺序中,锌>铁>氢>银,在硝酸亚铁和硝酸银的混合溶液中,加入一定量的锌,锌先与硝酸银反应生成了硝酸锌和银,若硝酸银完全反应锌再与硝酸亚铁反应生成了硝酸锌和铁,乙为无色溶液,说明硝酸亚铁和硝酸银全部参加化学反应,锌能与硝酸亚铁反应生成硝酸锌和铁,能与硝酸银反应生成硝酸锌和银,故固体甲中含有铁和银,可能有剩余的锌,发生反应的方程式是:Zn+Fe(NO3)2═Zn(NO3)2+Fe、Zn+2AgNO3═Zn(NO3)2+2Ag;
(2)若溶液乙为浅绿色溶液,说明了溶液中含有硝酸亚铁,锌完全发生了反应,溶液中一定含有硝酸锌、硝酸亚铁,可能含有硝酸银。所以溶液乙中溶质的组成可能是Zn(NO3)2、Fe(NO3)2或Zn(NO3)2、Fe(NO3)2、AgNO3。
故答案为:(1)铁、银;锌;Zn+Fe(NO3)2═Zn(NO3)2+Fe(或Zn+2AgNO3═Zn(NO3)2+2Ag)。
(2)Zn(NO3)2、Fe(NO3)2;Zn(NO3)2、Fe(NO3)2、AgNO3。

练习册系列答案
相关题目