题目内容
某同学向盛有少量碳酸钠溶液的烧杯中滴入氯化钙溶液,立即产生白色沉淀,过滤后得到澄清滤液,你认为滤液中含有哪些溶质?请你猜想,并设计实验来验证.
[猜想]:
猜想①:滤液中的溶质有________;
猜想②:滤液中的溶质有________;
猜想③:滤液中只有________.
[设计实验]:
请你设计实验方案来验证以上猜想,并将有关内容填写在以下实验报告的空格内.
| 实验步骤 | 实验现象及有关化学方程式 | 结论 |
| ________ | ________ | 猜想①正确 |
| ________ | ________ | 猜想②正确 |
| ________ | ________ | 猜想③正确 |
碳酸钠、氯化钠 氯化钙、氯化钠 氯化钠 取少量滤液于试管中,滴加稀盐酸 有气泡产生
Na2CO3+2HCl=2NaCl
+H2O+CO2↑ 取少量滤液于试管中,滴加碳酸钠溶液 有白色沉淀生成
CaCl2+Na2CO3=2NaCl
+CaCO3↓ 取少量滤液于两支试管中,分别滴加碳酸钠溶液和稀盐酸 没有明显的现象
分析:【猜想】根据该反应是碳酸钠和氯化钙反应,从可能一种过量或两者恰好完全反应,进行分析,
【设计实验】根据碳酸钠和盐酸反应会产生气泡,氯化钙和碳酸钠反应会产生沉淀进行分析.
解答:在氯化钙和碳酸钠反应时,可能两者恰好完全反应,也可能其中的一种过量,根据组合知识和该反应原理知道都会生成氯化钠,
故答案为:
猜想①:滤液中的溶质有碳酸钠、氯化钠;
猜想②:滤液中的溶质有氯化钙、氯化钠;
猜想③:滤液中只有氯化钠.
碳酸钠遇到盐酸会产生气泡,氯化钙遇到碳酸钠会产生白色的碳酸钙沉淀,故答案为:
点评:在解此类题时,首先要会根据过量问题进行正确的猜想,然后根据各种物质的性质选择有特征的实验选择试剂进行验证.
Na2CO3+2HCl=2NaCl
+H2O+CO2↑ 取少量滤液于试管中,滴加碳酸钠溶液 有白色沉淀生成
CaCl2+Na2CO3=2NaCl
+CaCO3↓ 取少量滤液于两支试管中,分别滴加碳酸钠溶液和稀盐酸 没有明显的现象
分析:【猜想】根据该反应是碳酸钠和氯化钙反应,从可能一种过量或两者恰好完全反应,进行分析,
【设计实验】根据碳酸钠和盐酸反应会产生气泡,氯化钙和碳酸钠反应会产生沉淀进行分析.
解答:在氯化钙和碳酸钠反应时,可能两者恰好完全反应,也可能其中的一种过量,根据组合知识和该反应原理知道都会生成氯化钠,
故答案为:
猜想①:滤液中的溶质有碳酸钠、氯化钠;
猜想②:滤液中的溶质有氯化钙、氯化钠;
猜想③:滤液中只有氯化钠.
碳酸钠遇到盐酸会产生气泡,氯化钙遇到碳酸钠会产生白色的碳酸钙沉淀,故答案为:
| 实验步骤 | 实验现象及有关化学方程式 | 结论 |
| 取少量滤液于试管中,滴加稀盐酸 | 有气泡产生 Na2CO3+2HCl=2NaCl +H2O+CO2↑ | 猜想①正确 |
| 取少量滤液于试管中,滴加碳酸钠溶液 | 有白色沉淀生成 CaCl2+Na2CO3=2NaCl +CaCO3↓ | 猜想②正确 |
| 取少量滤液于两支试管中,分别滴加碳酸钠溶液和稀盐酸 | 没有明显的现象 | 猜想③正确 |
点评:在解此类题时,首先要会根据过量问题进行正确的猜想,然后根据各种物质的性质选择有特征的实验选择试剂进行验证.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
 (2013?南通一模)珍珠粉常为消费者喜爱,然而一些不法分子用贝壳粉冒充珍珠粉销售.一研究性学习小组为了鉴定某珍珠粉的真假,进行了以下探究.
(2013?南通一模)珍珠粉常为消费者喜爱,然而一些不法分子用贝壳粉冒充珍珠粉销售.一研究性学习小组为了鉴定某珍珠粉的真假,进行了以下探究.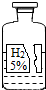 某同学在协助老师整理化学试剂时,发现一瓶标签残缺的无色溶液(如右图所示),此溶液是什么?对此问题他进行了如下探究.
某同学在协助老师整理化学试剂时,发现一瓶标签残缺的无色溶液(如右图所示),此溶液是什么?对此问题他进行了如下探究.