题目内容
铜粉和碳粉的混合物,在空气中充分加热后,生成的黑色物质与原混合物的质量相等,求铜在原混合物中的质量分数.
【答案】分析:欲正确解答本题,需知加热后2Cu+O2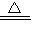 2CuO质量增加,C+O2
2CuO质量增加,C+O2 CO2变成气体放出,质量减少,由题意可知,生成的黑色物质与原混合物的质量相等,即原来的铜、碳混合物变成CuO,所以参加反应氧气的质量就是原混合物中碳的质量.然后根据化学方程式得出比例式,再根据质量分数公式计算即可.
CO2变成气体放出,质量减少,由题意可知,生成的黑色物质与原混合物的质量相等,即原来的铜、碳混合物变成CuO,所以参加反应氧气的质量就是原混合物中碳的质量.然后根据化学方程式得出比例式,再根据质量分数公式计算即可.
解答:解:由题意可知,生成的黑色物质与原混合物的质量相等,即原来的铜、碳混合物变成CuO,所以参加反应氧气的质量就是原混合物中碳的质量.也就是氧化铜中氧元素的质量就等于原混合物中碳的质量.
所以:铜的质量分数=: =80%,
=80%,
答:铜在原混合物中的质量分数为80%.
点评:本题主要考查学生对化学反应过程的了解情况,以及运用化学方程式进行计算的能力.
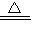 2CuO质量增加,C+O2
2CuO质量增加,C+O2 CO2变成气体放出,质量减少,由题意可知,生成的黑色物质与原混合物的质量相等,即原来的铜、碳混合物变成CuO,所以参加反应氧气的质量就是原混合物中碳的质量.然后根据化学方程式得出比例式,再根据质量分数公式计算即可.
CO2变成气体放出,质量减少,由题意可知,生成的黑色物质与原混合物的质量相等,即原来的铜、碳混合物变成CuO,所以参加反应氧气的质量就是原混合物中碳的质量.然后根据化学方程式得出比例式,再根据质量分数公式计算即可.解答:解:由题意可知,生成的黑色物质与原混合物的质量相等,即原来的铜、碳混合物变成CuO,所以参加反应氧气的质量就是原混合物中碳的质量.也就是氧化铜中氧元素的质量就等于原混合物中碳的质量.
所以:铜的质量分数=:
 =80%,
=80%,答:铜在原混合物中的质量分数为80%.
点评:本题主要考查学生对化学反应过程的了解情况,以及运用化学方程式进行计算的能力.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
铜粉和碳粉的混合物在空气中充分煅烧,所得固体产物与原混合物的质量相等,则原混合物中铜粉的质量分数为( )
| A、20% | B、84.5% | C、33.3% | D、80% |