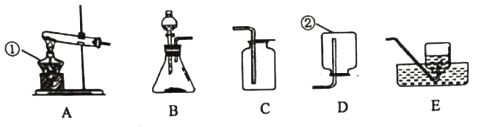题目内容
【题目】根据图回答下列问题:
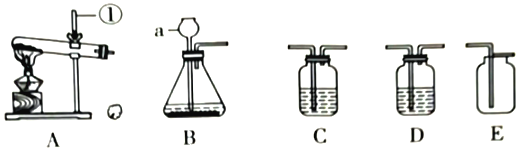
(1)写出标号仪器的名称:a_____。
(2)实验室里用B装置制取氧气,其反应的化学方程式为_____,实验时长颈漏斗的下端管口要伸入液面以下,其目的是_____。
(3)某实验小组用加热高锰酸钾制取氧气,应选用发生装置_____ (填序号);写出该反应的化学方程式:_____。
(4)若实验室用B装置制取二氧化碳,要收集纯净、干燥的二氧化碳气体,将实验装置按B→C→D→E顺序连接,则C装置内加入的试剂是_____,其作用是_____。
【答案】长颈漏斗 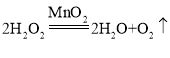 防止气体从长颈漏斗下端逸出 A
防止气体从长颈漏斗下端逸出 A ![]() 饱和碳酸氢钠溶液 吸收氯化氢
饱和碳酸氢钠溶液 吸收氯化氢
【解析】
(1)考查实验室常用仪器名称。
(2)过氧化氢在二氧化锰催化作用下分解生成水和氧气,据此书写化学方程式;根据装置气密性回答此题。
(3)根据高锰酸钾状态和反应条件选择发生装置;高锰酸钾在加热条件下反应生成锰酸钾、二氧化锰和氧气,据此书写化学方程式。
(4)根据二氧化碳气体中混有的杂质气体选择合适吸收剂。
(1)a为加入液体的长颈漏斗。
(2)过氧化氢在二氧化锰催化作用下分解生成水和氧气,化学方程式为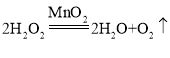 ;长颈漏斗下端不浸入液面以下,装置处于未密封状态,气体会从长颈漏斗下端逸出,故长颈漏斗的下端管口要伸入液面以下,可防止气体从长颈漏斗下端逸出。
;长颈漏斗下端不浸入液面以下,装置处于未密封状态,气体会从长颈漏斗下端逸出,故长颈漏斗的下端管口要伸入液面以下,可防止气体从长颈漏斗下端逸出。
(3)高锰酸钾为固体且反应需要加热,所以选择能加热的发生装置A;高锰酸钾在加热条件下反应生成锰酸钾、二氧化锰和氧气,化学方程式为![]() 。
。
(4)盐酸具有挥发性,所以二氧化碳气体中混有氯化氢气体,另外反应放热会带出水蒸气,因此二氧化碳气体中混有氯化氢和水蒸气,吸收氯化氢常用饱和碳酸氢钠溶液,水蒸气应最后被浓硫酸去除,保证气体干燥,所以C为吸收氯化氢的饱和碳酸氢钠溶液,作用是除去二氧化碳中的氯化氢气体。

 阅读快车系列答案
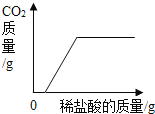
阅读快车系列答案【题目】将氯化钠和氯化铜的固体混合物30g完全溶于109.6 g水中形成溶液,再将100g一定溶质质量分数的氢氧化钠溶液分5次加入到该溶液中,充分反应后,测得的实验数据如下表所示:
实验次数 | 1 | 2 | 3 | 4 | 5 |
加入氢氧化钠溶液质量/g | 20 | 20 | 20 | 20 | 20 |
共生成沉淀的质量/g | 4.9 | 9.8 | m | 19.6 | 19.6 |
求:(1)表中m的值为 。
(2)原混合物中氯化铜的质量为 。
(3)恰好完全反应时,所得溶液的溶质质量分数是多少?(写出计算过程)
【题目】某校化学兴趣小组的同学在实验室对二氧化碳和澄清石灰水的反应进行再探究:在澄清石灰水中滴加无色酚酞试液溶液变成红色,将该红色溶液倒入充满二氧化碳的矿泉水瓶中。
[阅读资料]无色酚酞遇碱性物质变红色,遇酸性或中性物质不变色。
[实验现象]矿泉水瓶变瘪;溶液变红后又变为无色;溶液变浑浊后又变澄清。
[结论和解释]
矿泉水瓶变瘪的原因是_____;溶液由红色又变为无色的原因是_____;溶液变浑浊的化学方程式为_____;溶液由浑浊又变澄清让同学们产生了好奇,于是又做出以下猜想:是什么物质使溶液由浑浊又变澄清?
[提出猜想]猜想1:酚酞溶液
猜想2:二氧化碳
[设计实验]针对猜想1,你的验证实验方案是:_____。
针对猜想2,老师设计了以下分组实验,如表所示:
实验 | 操作 | 现象 |
方案一:向澄清石灰水中吹气 | 吹半分钟 | 澄清石灰水变浑浊 |
吹一分半钟 | 澄清石灰水变浑浊之后,又变澄清 | |
方案二:向集满CO2的集气瓶中滴加澄清石灰水 | 滴加1滴管 | 澄清石灰水变浑浊之后,又变澄清 |
滴加3滴管 | 澄清石灰水变浑浊 |
[表达与交流]方案一控制的变量是_____。
[得出结论]这两组对比实验得出_____不同,反应现象也不相同;还得出澄清石灰水由浑浊又变澄清和_____有关。
【题目】镁及其化合物在生产、生活中有着广泛的应用前景。
(一)镁及其化合物的广泛应用
(1)金属镁可以用于制造信号弹和焰火,因其燃烧时发出____
(2)工业上通过反应: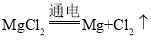 ,得到金属镁,反应中电能转化为___能
,得到金属镁,反应中电能转化为___能
(3)用不锈钢、合成橡胶、氧化镁等材料制造的飞机轮胎属于___材料。
(4)用含有Mg(OH)2的药物治疗胃酸过多,该反应的化学方程式为_________.
(5)碳酸镁可作阻燃剂,其可能的原因是____(选填序号)。
a 分解时吸热,降低可燃物的着火点
b 生成的固体覆盖燃烧物,隔绝氧气
(二)碳酸镁水合物的制备
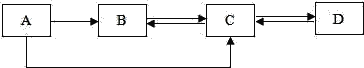
MgCO3· 3H2O是制备镁产品的中间体。工业上从碱性卤水(主要成分为MgCl2中获取MgCO3·3H2O的方法如图1所示。
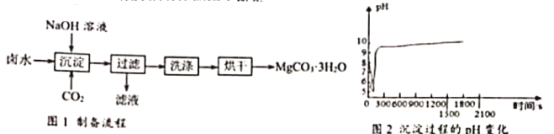
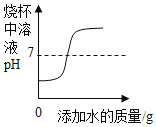
(1)“沉淀”过程的pH随时间的变化如图2所示,其操作为;向卤水中通入CO2至饱和然后滴加NaOH溶液,同时继续通入CO2,由此判断卤水的碱性比NaOH溶液_____(“强”或“弱”)。
(2)“沉淀”时生成MgCO3 ·3H2O的总反应化学方程式为_____
(3)证明沉淀已经洗涤干净的方法是:取最后一次洗涤所得滤液,先加足量稀HNO3滴加____溶液,无现象。
(三)样品成分的分析
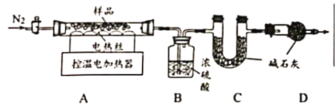
在烘干时,会有部分MgCO3·3H2O转化为碱式碳酸镁晶体Mga(OH)b(CO3)c · dH2O.为测定Mga(OH)b(CO3)c · dH2O的组成,称取18.46g固体混合物,在科研人员的指下用下图装置进行热分解实验,并记录实验数据于下表中。
温度/℃ | 室温 | 190 | 450 |
浓硫酸 | 150.00 | 155.40 | 156.30 |
碱石灰 | 100.00 | 100.00 | 106.16 |
(资料)
①MgCO3·3H2O在190℃完全失去结晶水;MgCO3;在400℃完全分解生成两种氧化物。
②Mga(OH)b(CO3)c · dH2O在210℃以下不分解:450℃完全分解生成三种氧化物。
(1)装配好实验装置后,先要______
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是__
(3)计算a:c=___,Mga(OH)b(CO3)c · dH2O中结晶水的质量为___g
(4)若实验中缺少D装置,则α:c的值____选填“偏大”、“偏小”或“不变”
(5)MgCO3·3H2O受热转化为碱式碳酸镁晶体Mga(OH)b(CO3)c · dH2O的化学方程式为______。