题目内容
【题目】某化学课外活动小组进行了一系列的实验探究,请按要求作答:

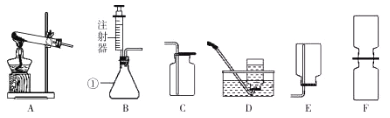
(1)实验室可用Zn粒和稀硫酸制H2,甲同学按图(1)所示配制实验所需的稀硫酸溶液,请你指出他操作中的两处错误.
(2)按要求从以下A﹣E装置中选择(填装置的字母序号).乙同学要制取并收集H2应选择 ;

(3)小松同学研究B装置后,作了改进,改进的装置如图(Ⅱ)所示.小松认为检查(Ⅱ)装置气密性的方法有以下三种:A打开止水夹a,手握住试管一会儿发现伸入水槽的导管口无汽泡冒出说明装置的气密性不好;B 先关闭止水夹a,往长颈漏斗里注水,当长颈漏斗内水面高于试管内水面时,停止加水,观察一段时间,发现长颈漏斗内、外水面高度差不变,说明装置的气密性好;C打开止水夹a,往长颈漏斗里注水,使长颈漏斗下管口在水面的上方,手握住液面以上的试管,发现伸入水槽的导管口无汽泡冒出,说明装置的气密性不好;你认为可行的方案是 (填序号).
(4)小松同学使用图(Ⅱ)装置实验室制取CO2,现有①Na2CO3固体、②块状大理石、③稀HCl和④稀H2SO4,应选用的试剂是 (填序号);反应进行过程中,关闭该装置中的止水夹a 后,可以观察到的现象是 .
(5)小亮同学也改进了B装置,改进的装置如图(Ⅲ)所示,与B装置相比较,图(Ⅲ)装置以分液漏斗代替长颈漏斗,其优点是 .
【答案】(1)将水倒入浓硫酸中;用量筒作为配制容器;
(2)BC(或BE);
(3)B;
(4)②③;液体被压回长颈漏斗中,固液分离,反应停止;
(5)能够控制反应速率.
【解析】解:(1)稀释浓硫酸时,一定要把浓硫酸沿着容器壁慢慢注入水中,同时用玻璃棒不断的搅拌,使产生的热量迅速散失,且配制溶液通常用烧杯,量筒不能用来配制溶液,只能用来量取液体的体积;
(2)实验室制取氢气用锌粒和稀硫酸常温反应,故选发生装置B,氢气密度比空气小且难溶于水,所以可用向下排空气法或排水法收集;
(3)检查该装置气密性的方法:A打开止水夹a,手握住试管一会儿发现伸入水槽的导管口无汽泡冒出说明装置的气密性不好;C打开止水夹a,往长颈漏斗里注水,使长颈漏斗下管口在水面的上方,手握住液面以上的试管,发现伸入水槽的导管口无汽泡冒出,说明装置的气密性不好;这两个选项都有两个出气口,气体受热膨胀也会从长颈漏斗逸出,故不可行;正确方法是B:先关闭止水夹a,往长颈漏斗里注水,当长颈漏斗内水面高于试管内水面时,停止加水,观察一段时间,发现长颈漏斗内、外水面高度差不变,说明装置的气密性好;
(4)实验室制取二氧化碳常用大理石和稀盐酸反应;关闭止水夹后,产生的气体不能出来,产生的压力使液体被压倒长颈漏斗中,固液分离,反应停止;
(5)与B装置相比较,图(Ⅲ)装置以分液漏斗代替长颈漏斗,可逐滴滴加液体,从而能够控制反应速率;
故答案为:
(1)将水倒入浓硫酸中;用量筒作为配制容器;
(2)BC(或BE);
(3)B;
(4)②③;液体被压回长颈漏斗中,固液分离,反应停止;
(5)能够控制反应速率.

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案