题目内容
【题目】下列有关叙述,对应的反应的化学方程式及基本类型均正确的是( )
A. 正常雨水的pH约为5.6的原因 SO2+H2O=H2SO3 化合反应
B. 用氢氧化钙中和硫酸的废水 Ca(OH)2+H2SO4=CaSO4+H2O 中和反应
C. 溶洞的形成 CaCO3+CO2+H2O=Ca(HCO3)2 化合反应
D. 工业上高炉炼铁:Fe2O3+3CO![]() 2Fe+3CO2 置换反应
2Fe+3CO2 置换反应
【答案】C
【解析】
A、正常雨水的pH约为5.6的原因是二氧化碳与水反应生成碳酸,正确的化学方程式为CO2+H2O=H2CO3,故A错误。
B、该化学方程式书写完全正确,但中和反应不是基本的反应类型,故B错误。
C、该化学方程式书写完全正确,该反应是则三种物质生成一种物质,属于化合反应,故C正确。
D、该化学方程式书写完全正确,但该反应的反应物均为化合物,不属于置换反应,故D错误。故选C。

 高中必刷题系列答案
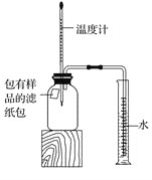
高中必刷题系列答案【题目】下图“黑面包”实验中,蔗糖(C12H22O11)变黑,体积膨胀,变成疏松的炭,放出有刺激性气味的气体。

(提出问题)改变糖的种类、浓硫酸的体积、水的滴数和温度是否会影响实验效果呢?
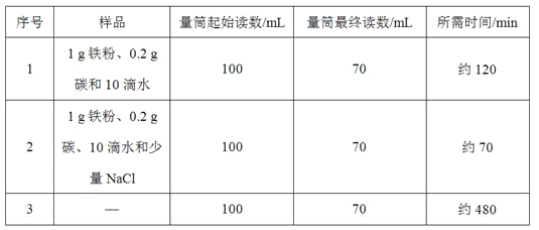
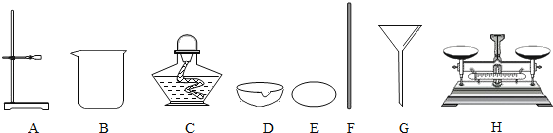
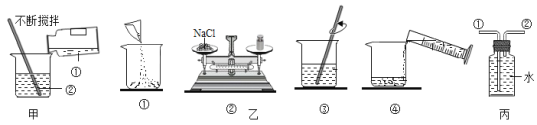
(进行实验)分别取5g糖粉进行实验,根据前2min的现象对实验效果进行评分,
记录如下:
表1实验记录
实验 | 糖 | 浓硫酸体积/mL | 水的滴数 | 温度/℃ | 效果得分 |
1 | 蔗糖 | 4 | 5 | 22 | 65 |
2 | 蔗糖 | 5 | 10 | 30 | 81 |
3 | 蔗糖 | 6 | 15 | 50 | 93 |
4 | 冰糖 | 4 | 10 | 50 | 91 |
5 | 冰糖 | 5 | 15 | 22 | 88 |
6 | 冰糖 | a | 5 | 30 | 75 |
7 | 葡萄糖 | 4 | 15 | 30 | 0 |
8 | 葡萄糖 | 5 | 5 | 50 | 0 |
9 | 葡萄糖 | 6 | 10 | 22 | 0 |
(处理数据)分析表1,计算效果得分均值,结果如下:
表2效果得分均值
因素 | 糖 | 浓硫酸体积/mL | 水的滴数 | 温度/℃ | ||||||||
蔗糖 | 冰糖 | 葡萄糖 | 4 | 5 | 6 | 5 | 10 | 15 | 22 | 30 | 50 | |
均值 | 79.7 | 84.7 | 0 | 52.0 | 56.3 | 56.0 | 46.7 | 57.3 | 60.3 | 51.0 | 52.0 | 61.3 |
依据均值推断最佳实验方案,均值越高,效果越好。
(解释与结论)
(1)蔗糖变成黑色的炭,发生了_____________(填“物理”或“化学”)变化。
(2)推测放出的气体含SO2,从元素守恒角度说明理由:________________________________。
(3)实验6中,a为_____________mL。
(4)根据表2推断,“黑面包”实验最好选择5g冰糖、5mL浓硫酸、_____滴水和50℃
(反思与评价)
(5)表2中,22℃对应的均值为51.0,计算该值所依据的3个数据分别是_____________________。
(6)综合分析,使实验3的效果得分高于实验4的因素有________________________________。
【题目】超市出现了一种名为“污渍爆炸盐”的洗新产品,能在瞬间去除洗衣粉难以除去的多种顽固污渍。某校化学兴趣小组的同学在老师的指导下对该产品开展了以下探究活动。

(阅读标签)本产品不含______,环保。
(查阅资料)①“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4),它是一种白色结晶颗粒,易溶于水,且能与水反应,生成碳酸盐和其他化合物。
②氢氧化镁是不溶于水的白色固体。
(提出问题)“污渍爆炸盐”水溶液的成分是什么呢?
(作出猜想)猜想一:Na2CO3和H2O2猜想二:Na2CO3和NaOH
猜想三:Na2CO3、H2O2和NaOH。
(实验探究)
序号 | 实验步骤 | 实验现象 | 实验结论 |
① | 取少量“污渍爆炸盐”于烧杯中,加入足量蒸馏水充分搅拌。 | 固体完全溶解形成无色溶液 | / |
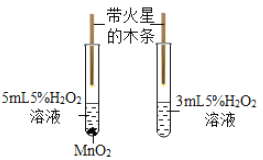
② | 取适量①的溶液于试管中,先向其中加入少量二氧化锰粉末,再将带火星的木条置于试管口 | 有大量气泡产生,木条复燃 | 含有______ |
③ | 取适量①的溶液于试管中,向其中加入足量_____,振荡、静置。 | 有白色淀产生 | 含有碳酸钠 |
④ | 取适量③的上层清液于试中,向其中滴加少量氯化镁溶液,振荡 | 清液中________ | 不含氢氧化钠 |
(得出结论)猜想______正确。
请写出过碳酸钠与水反应的化学方程式:______。
【题目】钙片的标签如图所示,且知此钙片成分中只有碳酸钙中含有钙元素,此标签中的含钙量是否正确?
(1)______(填“正确”或“错误”),为测定其含钙量,小东每次取10片钙片放入已称量的含足量稀盐酸的烧杯中,充分反应后再称取烧杯和剩余物的总质量,小东做了三次实验数据如下:
物质的质量 | 第1次 | 第2次 | 第3次 | 平均值 |
反应前:烧杯+稀盐酸 | 22g | 22g | 22g | 22g |
10片钙片 | 8g | 8g | 8g | 8g |
反应后:烧杯+稀盐酸 | 26.7g | 26.5g | 26.9g | 26.7g |
(2)每片钙片中含碳酸钙质量是____g
(3)通过小东的实验,你建议厂家如何修改标签?______。