题目内容
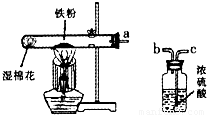
拉瓦锡曾经做了这样一个实验:让水蒸气通过一根烧红的枪管,生成了一种气体,难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,同学们设计了如图所示的装置进行探究.(1)已知试管内的湿棉花不参加反应,它的作用是______.
(2)若要干燥从a导管出来的气体,应从______(选填“b”或“c”)端管口通入;
(3)对该化学变化过程中生成的气体同学们有以下猜想:
猜想一:生成的气体可能是氢气.
猜想二:生成的气体可能是______.
(4)请你对猜想二进行探究:
| 操作方法 | 现象 | 结论 |
| ______ | ______ | ______ |
【答案】分析:(1)湿棉花含有水,在加热时对反应来说提供了水蒸气,据此分析解答即可;
(2)从洗气装置的操作原理分析;
(3)利用质量守恒定律、结合题干提供的问题对生成的气体分析判断;
(4)根据氧气的性质对相关实验进行设计;
(5)根据质量守恒定律及生成物的颜色分析.
解答:解:(1)由题意可知,要验证红热的铁能与水蒸气反应.由于湿棉花含有水,在加热时能形成水蒸气,所以湿棉花作用是:提供水蒸气;
(2)用浓硫酸来干燥气体,气体必须通入浓硫酸中,所以c进b出;
(3)根据质量守恒定律,反应物中只含Fe、O、H三种元素,生成的气体也就只有两种可能:H2或O2;
(4)氧气可以支持燃烧,鉴定氧气时常选用带火星的木条来进行鉴定;
(5)由质量守恒定律及生成物的颜色可知,四氧化三铁和氧化亚铁都是黑色的,生成的黑色固体可能是Fe3O4(或FeO、FeO与Fe3O4的混合物).
故答案是:
(1)提供反应所需水蒸气;(2)c;(3)氧气;
(4)
(5)Fe3O4(或FeO、FeO与Fe3O4的混合物).
点评:此题主要是考查了物质的性质和变化规律,答题时要紧扣题意,结合化学变化的本质及物质性质来考虑.
(2)从洗气装置的操作原理分析;
(3)利用质量守恒定律、结合题干提供的问题对生成的气体分析判断;
(4)根据氧气的性质对相关实验进行设计;
(5)根据质量守恒定律及生成物的颜色分析.
解答:解:(1)由题意可知,要验证红热的铁能与水蒸气反应.由于湿棉花含有水,在加热时能形成水蒸气,所以湿棉花作用是:提供水蒸气;
(2)用浓硫酸来干燥气体,气体必须通入浓硫酸中,所以c进b出;
(3)根据质量守恒定律,反应物中只含Fe、O、H三种元素,生成的气体也就只有两种可能:H2或O2;
(4)氧气可以支持燃烧,鉴定氧气时常选用带火星的木条来进行鉴定;
(5)由质量守恒定律及生成物的颜色可知,四氧化三铁和氧化亚铁都是黑色的,生成的黑色固体可能是Fe3O4(或FeO、FeO与Fe3O4的混合物).
故答案是:
(1)提供反应所需水蒸气;(2)c;(3)氧气;
(4)
| 操作方法 | 现象 | 结论 |
| 将带火星的木条放在b管口 | 带火星的木条复燃 | 说明该气体为氧气 |
点评:此题主要是考查了物质的性质和变化规律,答题时要紧扣题意,结合化学变化的本质及物质性质来考虑.

练习册系列答案
相关题目

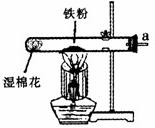
 20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.
20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.

 37、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如图所示的装置进行探究.
37、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如图所示的装置进行探究.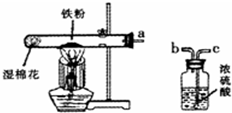 某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如右图所示的装置(浓硫酸起吸收水分干燥气体的作用)进行探究.
某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如右图所示的装置(浓硫酸起吸收水分干燥气体的作用)进行探究.