题目内容
【题目】根据题意回答。
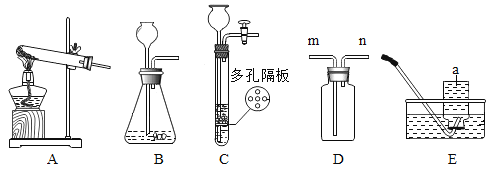
①写出仪器名称:a___________。
②实验室选用装置A制取氧气的化学方程式为___________,用装置E收集氧气验满的方法是________。
③实验室用大理石和稀盐酸制取二氧化碳可选用的发生装置是___________,若用装置D收集二氧化碳,则气体应从___________。(填“m”或“n”)端进入。
④装置C和装置B相比,其优点是___________,C中反应___________(填“进行中”或“已结束”)。
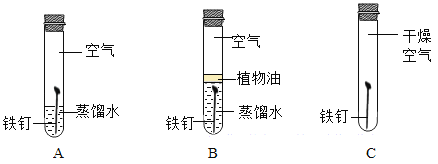
⑤下图所示实验G中铁丝不燃烧的原因是___________。
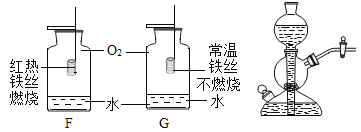
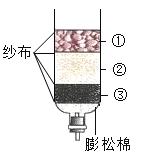
⑥启普发生器中,加入液体的量不能太少的理由是___________。
⑦含0.1摩尔碳酸钙的大理石与足量稀盐酸充分反应生成二氧化碳___________ g。(根据化学方程式列式计算)
【答案】集气瓶 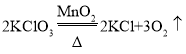 集气瓶有大量气泡出现 B或C m 随时控制反应的发生和停止 已结束 温度未达到铁丝着火点 液体的量太少,不能与固体反应物接触,反应不能进行 4.4;设含0.1摩尔碳酸钙的大理石与足量稀盐酸充分反应生成二氧化碳的物质的量为x,则:
集气瓶有大量气泡出现 B或C m 随时控制反应的发生和停止 已结束 温度未达到铁丝着火点 液体的量太少,不能与固体反应物接触,反应不能进行 4.4;设含0.1摩尔碳酸钙的大理石与足量稀盐酸充分反应生成二氧化碳的物质的量为x,则:
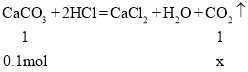
由![]() 解得x=0.1mol
解得x=0.1mol
0.1mol二氧化碳的质量为![]() 。
。
答:含0.1摩尔碳酸钙的大理石与足量稀盐酸充分反应生成二氧化碳4.4g。
【解析】
①图中仪器a是集气瓶;
②实验室选用装置A制取氧气,根据装置可知应该选择固体反应物,且反应条件为加热,那么可以选择加热分解氯酸钾制氧气,反应的化学方程式为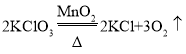 ,装置E为排水集气法收集气体,当看到瓶口有大气泡冒出时,说明氧气已经收集满;
,装置E为排水集气法收集气体,当看到瓶口有大气泡冒出时,说明氧气已经收集满;
③实验室用大理石和稀盐酸制取二氧化碳应该选择固液不加热型发生装置,图中可供选用的发生装置是B或C,若用装置D收集二氧化碳,由于二氧化碳的密度比空气密度大,用向上排空气法收集,则气体应从m端进入;
④装置C和装置B相比,其优点是可以随时控制反应的发生和停止,关闭止水夹,内气压增大,液体会与固体分离,反应停止,如图所示C中液体与固体已经分离开,说明反应已结束;
⑤物质燃烧需要三个条件:可燃物,与空气接触,温度达到着火点;G中常温下铁丝在氧气中不燃烧,原因是温度没有达到着火点;
⑥如图所示启普发生器中,加入液体的量太少,中央的固体反应物与液体不能接触,反应就不能进行;
⑦设含0.1摩尔碳酸钙的大理石与足量稀盐酸充分反应生成二氧化碳的物质的量为x,则:
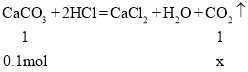
由![]() 解得x=0.1mol
解得x=0.1mol
0.1mol二氧化碳的质量为![]() 。
。
答:含0.1摩尔碳酸钙的大理石与足量稀盐酸充分反应生成二氧化碳4.4g。

【题目】下表为氯化钠和硝酸钾部分溶解度,请根据表中数据填空。
| 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
| 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
①溶解度单位是________。
②称取40g粗盐(含少量不溶于水的杂质)进行提纯。20℃时,将其溶解,取水量最适合的是_______g(选填“100”“110”或“120”)。溶解、过滤、蒸发得到精盐,上述三步中都要用到的实验仪器是________。
③20℃时,将硝酸钾进行如下实验过程:进行A-D四个步骤
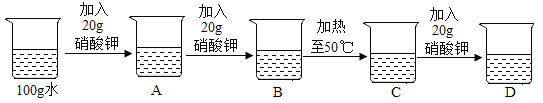
其中,C中为________(选填“饱和”“不饱和”)溶液,其中溶质质量分数最大的是________(选填A、B、C、D编号)。当D降温至10℃后,烧杯中得到硝酸钾固体________g,若要继续得到较多量的硝酸钾,易采用的结晶方法是_______(选填“蒸发”“降温”)。