题目内容
【题目】现有盐酸和 CaCl2 的混合溶液,向其中逐滴加入过量的碳酸钠溶液,溶液的pH 随滴入碳酸钠的量的变化关系如图所示。
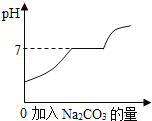
(1)向混合溶液中加入碳酸钠溶液,先发生的化学反应方程式为_____
(2)写出 pH=7 的过程中现象是_____。
(3)当 pH>7 时,溶液中阴离子的符号是 _____。
【答案】Na2CO3+2HCl=2NaCl+H2O+CO2↑ 有白色沉淀生成 Cl-、CO32-
【解析】
(1)碳酸钠首先与盐酸反应,反应完成后,碳酸钠再与氯化钙反应生成沉淀,所以先发生的化学反应方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;故填:Na2CO3+2HCl=2NaCl+H2O+CO2↑。
(2)pH=7时说明溶液中盐酸反应完毕,发生的是碳酸钠和氯化钙的反应,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,因此pH=7的过程中现象是:有白色沉淀生成;故填:有白色沉淀生成。
(3)碳酸钙和盐酸、氯化钙均发生反应,盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,碳酸钠和氯化钙反应生成碳酸钙和氯化钠,由图像可知,当pH>7时,此时溶液中溶质是氯化钠和过量的碳酸钠,阴离子是氯离子和碳酸根离子,为:Cl-、CO32-。故填:Cl-、CO32-。

【题目】分类、类比、推理都是学习化学常用的方法。
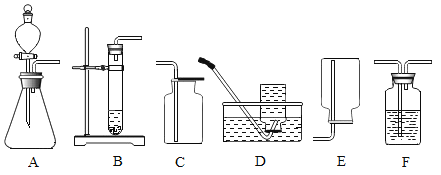
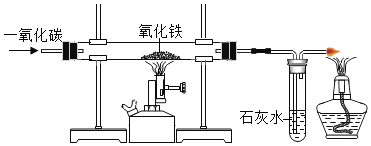
(1)物质的性质很大程度上决定了物质的用途,熟知物质的性质才能更好的应用物质,下图为初中化学教材中的实验。请回答问题:
A组 | B组 | 实验C | ||
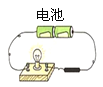
石墨导电实验 |
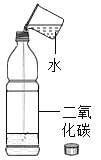
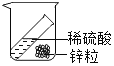
二氧化碳的溶解性实验 |
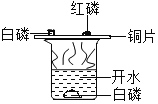
氢气燃烧 |
生石灰中加入水 |
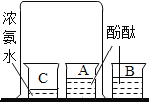
酸或碱的溶液改变花的颜色 |
若按照研究物质性质的角度进行分类,应将实验C归为_____组,理由是_____;
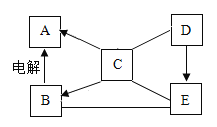
(2)通过课外阅读发现有下列反应:
Cl2+2NaBr=2NaCl+Br2 Br2+2KI=2KBr+I2
Cl2 Br2 I2 是氯、溴、碘三种元素组成的三种非金属单质。经过类比分析,发现非金属单质与盐发生的置换反应跟金属与盐发生的置换反应有类似的规律。因此可以判断Cl2 Br2 I2 三种非金属中活泼性最强的是_____(写化学式)。
查阅资料又得知结论:硫的活泼性比上述三种单质的活泼性都弱。请仿照上述反应,用硫元素和钾元素组成的化合物与其发生的一个反应来证明此结论(用化学方程式回答)_____。