题目内容
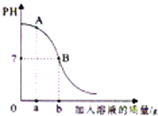
【题目】在一烧杯中盛有100g硫酸铜和硫酸的混合液,向其中逐渐滴加足量10%的氢氧化钠溶液,产生沉淀质量与滴入氢氧化钠溶液的关系,如图:请根据题意,回答下列问题:
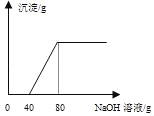
(1)在实验过程中,加入40g NaOH溶液时所得溶液中溶质为(写化学式)_____。
(2)在实验过程中加入80g NaOH溶液时,通过计算求此时所得不饱和溶液中溶质质量分数?_____(结果精确到0.1%)
【答案】Na2SO4、CuSO4 8.1%
【解析】
根据图可知,加入40g氢氧化钠溶液时才有氢氧化铜开始生成,所以此时有先前生成的硫酸钠以及尚未反应的硫酸铜,所以加入40g NaOH溶液时所得溶液中溶质的化学式为 Na2SO4、CuSO4。
与硫酸铜反应的氢氧化钠的质量为(80g﹣40g)×10%=4g
设生成的氢氧化铜沉淀的质量为x
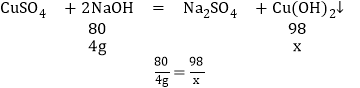
x=4.9g
设生成的硫酸钠的质量为y
根据钠元素守恒可得关系式为
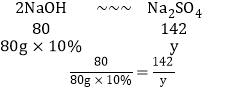
y=14.2g
此时所得不饱和溶液中溶质质量分数为![]() ×100%≈8.1%
×100%≈8.1%
答:(1)在实验过程中,加入40g NaOH溶液时所得溶液中溶质为 Na2SO4、CuSO4。
(2)在实验过程中加入80g NaOH溶液时,此时所得不饱和溶液中溶质质量分数为8.1%

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目