题目内容
【题目】一定条件下,xgCH4与16.0g O2恰好完全反应;生成水的同时得到CO和CO2的混合气体10.0g,经测定混合气体中碳元素的质量分数为36%,则参加反应的CH4与O2的质量之比为______________,其反应的化学方程式为_______________________。
【答案】3:10 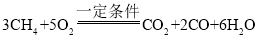
【解析】
混合气体中碳元素的质量分数为36%,故碳元素的质量=10.0g×36%=3.6g,而碳元素又全部来自CH4,可以计算出CH4的质量=![]() ,故参加反应的CH4与O2的质量之比为3:10。参加反应的甲烷与氧气的化学计量数之比=
,故参加反应的CH4与O2的质量之比为3:10。参加反应的甲烷与氧气的化学计量数之比=![]() ,甲烷和氧气反应生成水、二氧化碳和一氧化碳, 根据质量守恒定律以及化学方程式的书写方法可知,该反应的化学方程式为
,甲烷和氧气反应生成水、二氧化碳和一氧化碳, 根据质量守恒定律以及化学方程式的书写方法可知,该反应的化学方程式为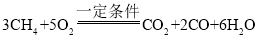 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】2020年一场抗击新冠肺炎的战疫在全球展开,一些消毒剂再次走进了百姓家。下表是几种消毒剂,请完成下列问题:
序号 | ① | ② | ③ | ④ |
消毒剂 | 医用酒精 | 二氧化氯 | 过氧乙酸 | “84”消毒液 |
主要成分 | C2H5OH | ClO2 | CH3COOOH | NaClO |
(1)其主要成分属于有机物的是_____(填序号,下同),属于氧化物的是_____。
(2)制备“84”消毒液主要成分次氯酸钠(NaCIO)的化学方程式为![]() ,则X的化学式为_____;次氯酸钠中氯元素的化合价是_____价。
,则X的化学式为_____;次氯酸钠中氯元素的化合价是_____价。
(3)过氧乙酸是一种无色透明的液体,有刺激性气味,易溶、挥发,易分解,有强酸性。
①用100g质量分数为10%的过氧乙酸溶液配制2%的该溶液,需水_____mL。
②下列关于过氧乙酸,说法正确的是_____(填序号)。
A 该物质可用于铁质容器的消毒
B 配制溶液时应帶橡胶手套,防止药液溅到皮肤上
C 如果药品不慎溅入眼中或皮肤上,应立即用氢氧化钠溶液冲洗
D 该物质适合长期放置使用
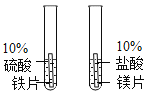
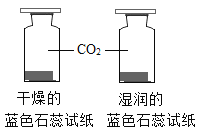
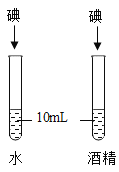
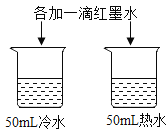
【题目】控制变量是实验探究的重要方法。下列实验设计不能达到实验目的的是( )
|
|
|
|
A.探究铁、镁金属活动性强弱 | B.探究二氧化碳与水是否发生反应 | C.探究不同溶剂中物质溶解性大小 | D.探究温度对分子运动快慢的影响 |
A. AB. BC. CD. D