题目内容
【题目】下图是某化学兴趣小组。设计的金属活动性顺序的探究实验。
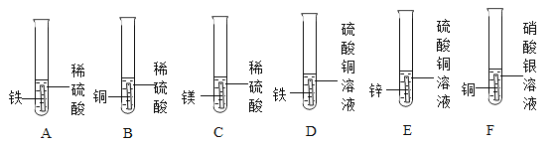
(1)上述实验中,有气泡生成的是________(填写装置序号)。
(2)试管F中出现的实验现象是_________________________________。
(3)上述实验能否证明镁、锌、铁、铜、银五种金属的活动性强弱?_____。
(4)我国古代“湿法炼铜”就是利用了试管D中的反应原理,请写出该反应的化学方程式:_____________________;该反应的基本类型是________________。
【答案】A、C有白色固体出现,溶液由无色变为蓝色不能Fe+CuSO4=Cu+FeSO4置换反应
【解析】
(1)镁、铁排在氢的前面,能与稀硫酸反应生成氢气;
(2)铜和硝酸银反应生成银和硝酸铜,反应的现象为:有白色固体出现,溶液由无色变为蓝色;
(3)通过金属和酸溶液的反应,可以判断出铁和镁都在氢前;通过金属和盐溶液的反应,可以判断出铁和锌都在铜前,铜在银前,但最终不能判断出镁、锌、铁间的金属活动性顺序;
(4)铁和硫酸铜溶液反应生成硫酸亚铁和铜,其反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;由于是一种单质和一种化合物,生成另一种单质和另一种化合物的反应,所以属于置换反应。

 阅读快车系列答案
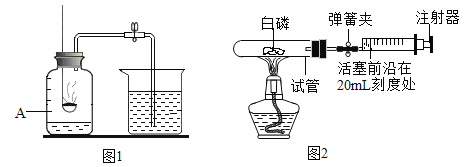
阅读快车系列答案【题目】如图是测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题。
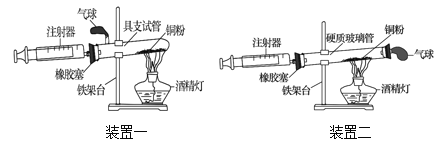
(1)根据下表提供的实验数据,完成下表。
硬质玻璃管中 空气的体积 | 反应前注射器 中空气体积 | 反应后注射器 中气体体积 | 实验测得空气 中氧气的体积分数 |
25mL | 15mL | 9mL | _____ |
(2)装置一和装置二中气球的位置不同,_____ (填“装置一”或“装置二”)更合理,理由是_____。
(3)若实验测得的结果偏小(氧气的体积分数小于 21%),可能的原因有哪些?(列举两条)
①_________________;②____________。