题目内容
【题目】四会江河众多,四方之水交错汇流,而称“四会”。其中绥江之水贯城而过,水质优美,形成独特的风景。
(1)为了检验绥江河水是软水还是硬水,可向水样中加入_____,搅拌,如果观察到水样中泡沫很少,有沉淀析出,则为硬水,如果泡沫很多,也没有沉淀析出,则为软水。在日常生活中,常采用_____的方法降低水的硬度。
(2)绥江之滨,有座贞山,草木茂盛,泉水众多。下列说法中错误的是_____(填序号)
A清澈的泉水肯定属于纯净物
B过滤不可以除去泉水中的所有杂质
C水的天然循环实现了自身的净化
D水是一种常用的溶剂
(3)泉水中蕴含一定量的钾元素与钠元素。已知KNO3和NaCl都是易溶于水的物质,它们的溶解度曲线如图所示:
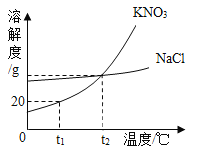
①t1℃时,KNO3饱和溶液的溶质质量分数_____NaCl饱和溶液的质量分数(填“大于”“小于”“等于”之一)。
②t2℃时,向盛有50g水的烧杯中加入50g KNO3充分溶解后,缓慢降温至t1℃,则所得溶液中溶质与溶液的质量比是_____(填最简整数比)。
③当KNO3固体中含有少量NaCl时,可采用冷却结晶的方法提纯KNO3,请说明提纯的原理:_____。
【答案】肥皂水 煮沸 A 小于 1:6 KNO3溶解度随温度降低明显变小,而NaCl溶解度随温度降低变化不明显,故降温时,KNO3大量析出
【解析】
根据水的净化的知识进行分析解答,根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
(1)检验硬水和软水使用的是肥皂水,要将硬水软化,可以采用煮沸的方法降低水的硬度,故填写:肥皂水;煮沸;
(2)A、清澈的泉水不属于纯净物,选项说法错误,故符合题意;
B、过滤不可以除去泉水中的所有杂质,选项说法正确,故不符合题意;
C、水的天然循环实现了自身的净化,选项说法正确,故不符合题意;
D、水是一种常用的溶剂,选项说法正确,故不符合题意,故填写:A;
(3)①t1℃时,硝酸钾的溶解度小于氯化钠,故KNO3饱和溶液的溶质质量分数小于NaCl饱和溶液的质量分数,故填写:小于;
②t2℃时,向盛有50g水的烧杯中加入50g KNO3充分溶解后,缓慢降温至t1℃,该温度下硝酸钾的溶解度为20g,形成的是饱和溶液,则所得溶液中溶质与溶液的质量比是10g:60g=1:6,故填写:1:6;
③当KNO3固体中含有少量NaCl时,可采用冷却结晶的方法提纯KNO3,是因为KNO3溶解度随温度降低明显变小,而NaCl溶解度随温度降低变化不明显,故降温时,KNO3大量析出,故填写:KNO3溶解度随温度降低明显变小,而NaCl溶解度随温度降低变化不明显,故降温时,KNO3大量析出。

 阅读快车系列答案
阅读快车系列答案【题目】化学就在我们身边,人类的生活离不开化学。
(1)在人类食物所供给的总能量中,有 60%~70%来自_____。
(2)烹饪过程中使用了加碘盐,其目的是防止缺碘引起__________填“甲状腺肿大”、“贫 血”或“佝偻病”)。
(3)炉具清洁剂中氢氧化钠去除油污的原理是____________。
(4)乙醇可用作酒精灯、内燃机等的燃料,写出乙醇充分燃烧的化学方程式:_________。
(5)化肥对提高农作物的产量具有重要作用。请用化学方法完成鉴别尿素和硝酸铵两种固 体化肥的实验报告。
实验步骤 | 实验现象 | 实验结论 |
____________ | _____________ | ________________ |
【题目】某同学设计了下表中的三组实验,分别向甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用下图曲线表示的是()
甲 | 乙 | |
① | 银、锌的混合物 | 稀盐酸 |
② | 硫酸和硫酸镁的混合溶液 | 氢氧化钡溶液 |
③ | 盐酸和氯化铵的浓溶液 | 氢氧化钠浓溶液 |
④ | 生锈的铁钉 | 稀盐酸 |

A.①②B.③④C.②④D.②③④