题目内容
【题目】用化学符号表示下列化学反应:
(1)有大量白烟生成的化合反应:_____。
(2)有黑色固体生成的化合反应:_____。
(3)有水生成的分解反应:_____。
(4)实验室用加热混合物的方法制取氧气:_____。
(5)甲烷(CH4)在空气中燃烧生成二氧化碳和水:_____。
【答案】P+O2![]() P2O5或NH3+HCl→NH4Cl Fe+O2
P2O5或NH3+HCl→NH4Cl Fe+O2![]() Fe3O4或Cu+O2
Fe3O4或Cu+O2![]() CuO H2O2
CuO H2O2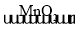 H2O+O2 KClO3
H2O+O2 KClO3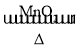 KCl+O2 CH4+O2
KCl+O2 CH4+O2![]() CO2+H2O
CO2+H2O
【解析】
(1)由两种或两种以上的物质生成一种物质的反应叫化合反应,有大量白烟生成的化合反应:P+O2![]() P2O5或NH3+HCl→NH4Cl;
P2O5或NH3+HCl→NH4Cl;
(2)有黑色固体生成的化合反应:Fe+O2![]() Fe3O4或Cu+O2
Fe3O4或Cu+O2![]() CuO,氧化铜和四氧化三铁是黑色固体;
CuO,氧化铜和四氧化三铁是黑色固体;
(3)由一种物质生成两种或两种以上物质的反应叫分解反应,有水生成的分解反应:H2O2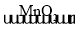 H2O+O2或H2CO3
H2O+O2或H2CO3![]() CO2+H2O;
CO2+H2O;
(4)实验室用氯酸钾法制氧气,是加热混合物的方法制取氧气:KClO3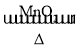 KCl+O2;
KCl+O2;
(5)甲烷(CH4)在空气中燃烧即甲烷和氧气在点燃条件下生成二氧化碳和水:CH4+O2![]() CO2+H2O。
CO2+H2O。

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案【题目】某同学设计如下几组实验,探究盐酸的性质。
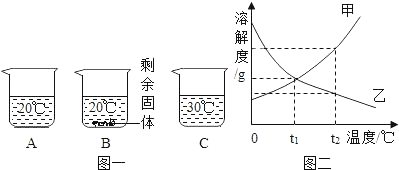
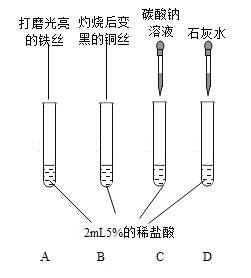
(第一组)选取3种溶液,2种固体,如下图所示进行实验。
实验 | 现象及结论 | 解释 |
| (1)试管A中产生______(填实验现象)。发生的反应类型是____。 | |
试管B可观察到铜丝外面的黑色逐渐消失。 | (2)试管B中增加的离子是__(填离子符号)。 | |
试管C中有气泡产生。复分解反应已发生。 | (3)反应的化学方程式为____。 |
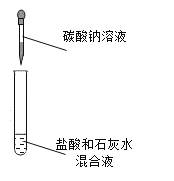
(第二组)对试管D中盐酸和氢氧化钙是否发生反应进行探究。如下图所示进行实验。
实验 | 现象及结论 | 解释 |
| 有白色沉淀产生,证明氢氧化钙溶液和稀盐酸的反应已发生。 | (4)你认为这个实验设计是否合理______,原因是_____。 |
通过测定D试管反应前后溶液的pH变化,确定发生反应。 | ||
结论 | 氢氧化钙和盐酸能发生反应 | |
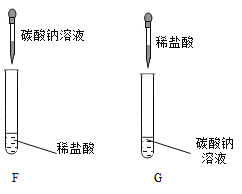
(第三组)对碳酸钠和稀盐酸的反应本质继续探究。如下图所示进行实验。
实验 | 现象及结论 | 解释 |
| 试管F中立刻有较多气泡产生。试管G中开始只有极少量气泡,一段时间后有较多气泡产生。 |
(5)试管G中一开始气泡很少的原因是____。 |
结论:盐酸能与铁、氧化铜、氢氧化钙、碳酸钠发生化学反应