题目内容
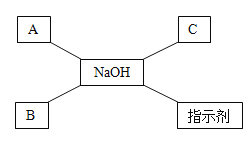
【题目】如图,碳化铝(又叫三碳化四铝)是黄色或绿灰色粉末,常用于冶金。以下框图表示的是与碳化铝有关的制备和性质的反应。


已知:G属于碱类,B属于金属单质,E在常温下为液体,F的相对分子质量小于24,试根据框图回答:
(1)E的化学式______,G的化学式______;
(2)①反应的化学方程式______;
(3)③反应的化学方程式______。
【答案】H2O Al(OH)3 ![]()
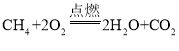
【解析】
根据A与B反应生成碳化铝和D,可知B为铝,而碳化铝含有碳元素,所以A中含有碳元素,E与碳化铝反应生成F和G,G为碱,说明含有氢氧根,氢元素和氧元素只能由E提供,常温下为液体,所以可以推测E为水,水和碳化铝反应生成G和F,G中有了氢氧根离子,还缺少金属离子,组成碱,所以G中含有铝元素,因此G为氢氧化铝,E与碳化铝含有铝、碳、氢、氧四种元素,G中含量铝、氢、氧三种元素,则F至少含有碳元素,但是若只有碳元素,与氧气不能生成E水,所以F中还应有氢元素,由于F相对分子质量小于24,所以其除了碳、氢元素外,不能再有其他元素,碳元素与氢元素可以组成甲烷,所以F为甲烷,甲烷与氧气反应生成水和二氧化碳,所以D为二氧化碳,而A与B反应生成碳化铝和D,此时生成物含有铝、碳、氧三种元素,而B中含有铝元素,所以A中含有碳和氧两种元素,所以推出A为一氧化碳,因此A为一氧化碳,B为铝,D为二氧化碳,E为水,F为甲烷,G为氢氧化铝。
解:(1)根据分析可知,E为水,化学式为H2O,G为氢氧化铝,化学式为Al(OH)3;
故答案为:H2O;Al(OH)3。
(2)①为一氧化碳与铝在加热条件下反应生成碳化铝和二氧化碳,书写化学方程式注意配平;
故答案为:![]() 。
。
(3)③为甲烷与氧气在点燃条件下反应生成二氧化碳和水,书写化学方程式注意配平;
故答案为: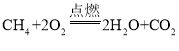 。
。

 53随堂测系列答案
53随堂测系列答案【题目】物质除杂是化学实验中经常遇到的问题。
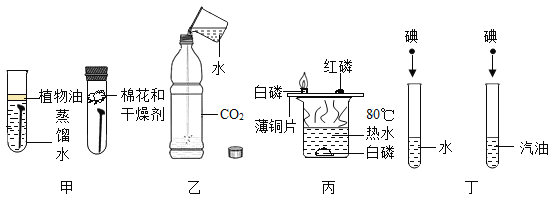
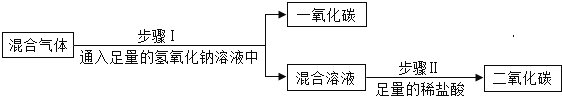
实验一:为除去二氧化碳气体中混有的少量一氧化碳,小明设计了三种方案。
实验方案 | |
方案 A |
|
方案 B |
|
方案 C |
|
上述方案中有两个方案是合理的,他们是___________写出合理方案中任意一个反应的化学方程式 ____________。
实验二:由于粗盐中含有少量 MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图:
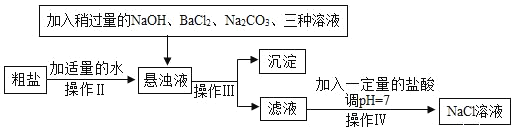
(1)加入稍过量的 Na2CO3溶液除了能除去粗盐中的 CaCl2外,它还有一个作用是 _____________(用化学方程式表示)
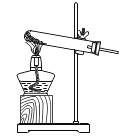
(2)实验操作Ⅲ是_____________,要用到的实验玻璃仪器是玻璃棒、漏斗和 ________________。
(3)如果稍过量的试剂加入的顺序依次为:Na2CO3、 NaOH、 BaCl2和盐酸,则最后得到的氯化钠溶液中一定含有杂质________________。
(4)操作Ⅳ的方法可以是:先在滤液中滴入酚酞溶液,再逐滴滴入盐酸直到滤液的 pH=7 的依据的现象是溶液由____________,如果加入的盐酸有点过量了,对后面 NaCl 溶液的结晶是否有影响______(是或否)