题目内容
化学是研究物质的,而物质是由肉眼看不到的分子、原子和离子等微观粒子构成的,让我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界.(1)金秋十月,丹桂飘香,我能从分子的角度分析其原因是
(2)下图是某反应的微观示意图,依据此图回答下列问题:

反应物中化合物的化学式为
(3)元素周期表是我们学习化学的重要工具.下表是小丽同学绘制的元素周期表的局部,依据此表回答问题:
| 1 H 氢 |
2 氦 | ||||||
| 3 锂 |
4 铍 |
5 硼 |
6 C 碳 |
7 N 氮 |
8 O 氧 |
9 F 氟 |
10 氖 |
| 11 Na 钠 |
12 Mg 镁 |
13 Al 铝 |
14 SI 硅 |
15 P 磷 |
16 S 硫 |
17 Cl 氯 |
18 氩 |
②地壳中含量最多的元素原子的质子数是
③磷元素在元素周期表中位于第

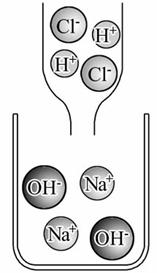
(4)右图是两种溶液恰好完全反应的微观示意图,我能写出此反应的化学方程式
分析:(1)闻到气味说明分子不断运动;
(2)根据分子模型判断物质的化学式,然后写出化学方程式,再根据反应前后原子的数目和种类不变获取信息;
(3)①根据元素符号的书写原则判断;②地壳中含量最多的元素是氧元素;③根据磷在元素周期表中的位置回答;
(4)根据粒子模型判断物质的化学式,然后写出化学方程式,根据生成物的构成判断存在的粒子.
(2)根据分子模型判断物质的化学式,然后写出化学方程式,再根据反应前后原子的数目和种类不变获取信息;
(3)①根据元素符号的书写原则判断;②地壳中含量最多的元素是氧元素;③根据磷在元素周期表中的位置回答;
(4)根据粒子模型判断物质的化学式,然后写出化学方程式,根据生成物的构成判断存在的粒子.
解答:解:(1)闻到花香,从分子的角度分析其原因是分子在不断运动.
(2)由反应的微观示意图可知,反应物中化合物的化学式为 CH4,反应的化学方程式为:CH4+2O2
CO2+2H2O,故生成物中各物质的粒子个数比是 1:2,从微观的角度还能获得一条关于物质变化的信息是化学反应前后,原子的种类和数目都没有改变.
(3)硅的元素符号应该是Si,不是SI,不符合书写原则;
②地壳中含量最多的元素的氧元素,氧原子的质子数是 8,它最外层有6个电子,在化学反应中它易得到电子.
③由元素周期表可知,磷元素在元素周期表中位于第三周期.
(4)根据两种溶液恰好完全反应的微观示意图,反应物的HCl和NaOH,生成物是NaCl和H2O,反应的化学方程式为HCl+NaOH=NaCl+H2O;反应后所得溶液是NaCl溶液,其中含有的粒子有 Na+、Cl-、H2O.
故答案为:(1)分子在不断地运动
(2)CH4 1:2(或2:1)化学反应前后,原子的种类和数目都没有改变(或“原子是化学变化中的最小粒子”;“化学变化的实质是分子破裂和原子的重新组合”等;
(3)Si,8,得到,三;
(4)HCl+NaOH═NaCl+H2O Na+、Cl-、H2O
(2)由反应的微观示意图可知,反应物中化合物的化学式为 CH4,反应的化学方程式为:CH4+2O2
| ||
(3)硅的元素符号应该是Si,不是SI,不符合书写原则;
②地壳中含量最多的元素的氧元素,氧原子的质子数是 8,它最外层有6个电子,在化学反应中它易得到电子.
③由元素周期表可知,磷元素在元素周期表中位于第三周期.
(4)根据两种溶液恰好完全反应的微观示意图,反应物的HCl和NaOH,生成物是NaCl和H2O,反应的化学方程式为HCl+NaOH=NaCl+H2O;反应后所得溶液是NaCl溶液,其中含有的粒子有 Na+、Cl-、H2O.
故答案为:(1)分子在不断地运动
(2)CH4 1:2(或2:1)化学反应前后,原子的种类和数目都没有改变(或“原子是化学变化中的最小粒子”;“化学变化的实质是分子破裂和原子的重新组合”等;
(3)Si,8,得到,三;
(4)HCl+NaOH═NaCl+H2O Na+、Cl-、H2O
点评:此题考查了学生对微观粒子的理解和运用,从粒子的性质,反应过程,元素周期表和在溶液中的存在形式等方面设计问题,全面而具体,是一道很好的试题.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目


 (2012?株洲模拟)化学是研究物质的,而物质是由肉眼看不到的分子、原子和离子等微观粒子构成的,让我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界.如图是两种溶液恰好完全反应的微观示意图,我能写出:
(2012?株洲模拟)化学是研究物质的,而物质是由肉眼看不到的分子、原子和离子等微观粒子构成的,让我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界.如图是两种溶液恰好完全反应的微观示意图,我能写出: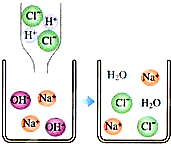 化学是研究物质的,而物质是由肉眼看不到的分子、原子和离子等微观粒子构成的,让我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界.
化学是研究物质的,而物质是由肉眼看不到的分子、原子和离子等微观粒子构成的,让我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界.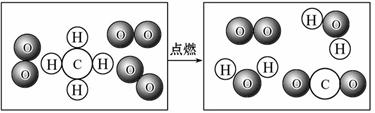
 为________,生成物中各物质的粒子个数比是______,从微观的角度还能获得一条关于物质变化的信息是_______________________
为________,生成物中各物质的粒子个数比是______,从微观的角度还能获得一条关于物质变化的信息是_______________________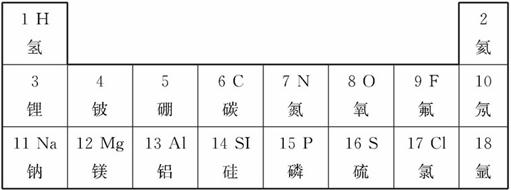
 _____________________,反应后所得溶液中含有的粒子有_______(填符号)。
_____________________,反应后所得溶液中含有的粒子有_______(填符号)。