题目内容
36、有一包粉末,可能由Ca(OH)2、K2SO4、CuCl2、Na2CO3中的一种或几种物质组成.现做如下实验:
实验1:取少量粉末,加水溶解后得到无色透明溶液.
实验2:取少量的实验1中所得溶液,加入无色酚酞,溶液呈红色.
实验3:取少量的实验1中所得溶液,滴入稀盐酸,有气泡产生.
根据以上实验,请回答:
(1)原粉末中一定没有
(2)原粉末中可能有
实验1:取少量粉末,加水溶解后得到无色透明溶液.
实验2:取少量的实验1中所得溶液,加入无色酚酞,溶液呈红色.
实验3:取少量的实验1中所得溶液,滴入稀盐酸,有气泡产生.
根据以上实验,请回答:
(1)原粉末中一定没有
CuCl2 Ca(OH)2
,一定有Na2CO3
.(2)原粉末中可能有
K2SO4
,为了验证可能含有的成分是否存在,请你设计实验证明:| 操作 | 现象 | 结论 |
取样,加入氯化钡溶液和稀硝酸 |
有沉淀产生 |
有K2SO4 |
分析:(1)根据铜离子在溶液中显蓝色进行分析,氢离子会与碳酸根离子生成气体,碳酸根离子会与钙离子生成生成沉淀进行分析.
(2)根据实验1、2、3中的现象进行分析.
根据硫酸根离子会与钡离子生成沉淀进行分析.
(2)根据实验1、2、3中的现象进行分析.
根据硫酸根离子会与钡离子生成沉淀进行分析.
解答:解:(1)氯化铜在溶液中显蓝色,而固体加水后是无色透明溶液,一定没有氯化铜,取少量的实验1中所得溶液,滴入稀盐酸,有气泡产生,一定存在碳酸钠,碳酸钠会与氢氧化钙生成白色沉淀,所以没有氢氧化钙,故答案为:CuCl2、Ca(OH)2;Na2CO3;
(2)从实验现象不能确定硫酸钾的存在或不存在,故答案为:K2SO4;
硫酸根离子会与钡离子生成白色的硫酸钡沉淀,可以加入硝酸酸化的氯化钡检验硫酸钾的存在,故答案为:
(2)从实验现象不能确定硫酸钾的存在或不存在,故答案为:K2SO4;
硫酸根离子会与钡离子生成白色的硫酸钡沉淀,可以加入硝酸酸化的氯化钡检验硫酸钾的存在,故答案为:
| 操作 | 现象 | 结论 |
| 取样,加入氯化钡溶液和稀硝酸 | 有沉淀产生 |
有K2SO4 |
点评:在解此类题时,首先根据题中的现象确定存在或不存在的物质,对于现象不能确定的,还需要设计实验进行验证.

练习册系列答案
相关题目
有一包粉末,可能由C、CuO、Fe三种物质中的一种或两种组成.小明同学为了探究它的成分,按如下步骤进行实验.
(1)小明先对实验做了如下设想和分析.取少量粉末于烧杯中,向烧杯中加入过量的稀硫酸,则实验中可能出现的现象与对应结论如下表所示(表中未列完所有情况).请你帮助完成.
(2)通过实验及分析,确定该粉末为C、CuO的混合物.小方想继续探究:木炭在高温条件与氧化铜反应生成的红色粉末的组成.
【查阅资料】①Cu、Cu2O都是红色固体;
②2CuO+C
2Cu+CO2↑,4CuO
2Cu2O+O2↑
③CO+Cu2O
2Cu+CO2,Cu2O+2HCl=CuCl2+Cu+H2O
【猜想】生成的红色粉末究竟是什么?请你和小方一起完成下列猜想:
猜想①Cu; 猜想②Cu2O; 猜想③ .
【设计实验】小方同学设计了一个简单实验很快排除了猜想①,请你帮助他完成下表:
为进一步确定红色粉末的组成,小方利用下列装置,设计了如下实验方案(装置气密性良好).
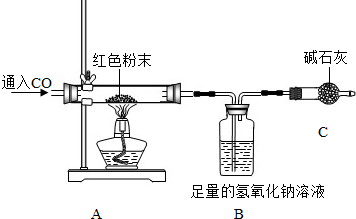
①取红色粉末样品的质量20克; ②测出反应前B装置的总质量为210.0克;
③反应很长时间后测得B装置的总质量为214.4克;④通过计算确定红色粉末的组成.
根据上述实验,回答下列问题:
Ⅰ.实验开始时,先通CO后称量B装置的总质量,再加热,实验目的是
A.排尽装置内空气,防止加热发生爆炸
B.防止装置内的空气影响测量结果
C.防止液体倒流到硬质玻璃管中
Ⅱ.C装置的作用是 .
Ⅲ.为防止实验中尾气对大气的污染,可以对尾气进行收集,现提供水槽和集气瓶,还需一种仪器是 .
Ⅳ.请你根据以上数据通过计算,得出红色粉末组成是 .
Ⅴ.不改变装置和药品,你还可以通过测定 等数据,再通过计算得出红色粉末组成.
【交流反思】小红认为红色粉中的铜,有一部分可能是C与Cu2O在高温下反应生成的,写出反应的化学方程式: .
(1)小明先对实验做了如下设想和分析.取少量粉末于烧杯中,向烧杯中加入过量的稀硫酸,则实验中可能出现的现象与对应结论如下表所示(表中未列完所有情况).请你帮助完成.
| 烧杯中可能出现的现象 | 结论 |
| ①有黑色不溶物,无气泡逸出,溶液呈无色 | 结论:只含 |
| ② |
结论:含C、CuO |
| ③ |
结论:含C、Fe |
【查阅资料】①Cu、Cu2O都是红色固体;
②2CuO+C
| ||
| ||
③CO+Cu2O
| ||
【猜想】生成的红色粉末究竟是什么?请你和小方一起完成下列猜想:
猜想①Cu; 猜想②Cu2O; 猜想③
【设计实验】小方同学设计了一个简单实验很快排除了猜想①,请你帮助他完成下表:
| 实验步骤 | 现象 | 结论 |
| 猜想①不正确 |

①取红色粉末样品的质量20克; ②测出反应前B装置的总质量为210.0克;
③反应很长时间后测得B装置的总质量为214.4克;④通过计算确定红色粉末的组成.
根据上述实验,回答下列问题:
Ⅰ.实验开始时,先通CO后称量B装置的总质量,再加热,实验目的是
A.排尽装置内空气,防止加热发生爆炸
B.防止装置内的空气影响测量结果
C.防止液体倒流到硬质玻璃管中
Ⅱ.C装置的作用是
Ⅲ.为防止实验中尾气对大气的污染,可以对尾气进行收集,现提供水槽和集气瓶,还需一种仪器是
Ⅳ.请你根据以上数据通过计算,得出红色粉末组成是
Ⅴ.不改变装置和药品,你还可以通过测定
【交流反思】小红认为红色粉中的铜,有一部分可能是C与Cu2O在高温下反应生成的,写出反应的化学方程式:
有一包粉末,可能由C、CuO、Fe三种物质中的一种或两种组成.小明同学为了探究它的成分,按如下步骤进行实验.
(1)小明先对实验做了如下设想和分析.取少量粉末于烧杯中,向烧杯中加入过量的稀硫酸,则实验中可能出现的现象与对应结论如下表所示(表中未列完所有情况).请你帮助完成.
(2)通过实验及分析,确定该粉末为C、CuO的混合物.小方想继续探究:木炭在高温条件与氧化铜反应生成的红色粉末的组成.
【查阅资料】①Cu、Cu2O都是红色固体;
②2CuO+C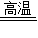 2Cu+CO2↑,4CuO
2Cu+CO2↑,4CuO 2Cu2O+O2↑
2Cu2O+O2↑
③CO+Cu2O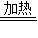 2Cu+CO2,Cu2O+2HCl=CuCl2+Cu+H2O
2Cu+CO2,Cu2O+2HCl=CuCl2+Cu+H2O
【猜想】生成的红色粉末究竟是什么?请你和小方一起完成下列猜想:
猜想①Cu; 猜想②Cu2O; 猜想③______.
【设计实验】小方同学设计了一个简单实验很快排除了猜想①,请你帮助他完成下表:
为进一步确定红色粉末的组成,小方利用下列装置,设计了如下实验方案(装置气密性良好).

①取红色粉末样品的质量20克; ②测出反应前B装置的总质量为210.0克;
③反应很长时间后测得B装置的总质量为214.4克;④通过计算确定红色粉末的组成.
根据上述实验,回答下列问题:
Ⅰ.实验开始时,先通CO后称量B装置的总质量,再加热,实验目的是______
A.排尽装置内空气,防止加热发生爆炸
B.防止装置内的空气影响测量结果
C.防止液体倒流到硬质玻璃管中
Ⅱ.C装置的作用是______.
Ⅲ.为防止实验中尾气对大气的污染,可以对尾气进行收集,现提供水槽和集气瓶,还需一种仪器是______.
Ⅳ.请你根据以上数据通过计算,得出红色粉末组成是______.
Ⅴ.不改变装置和药品,你还可以通过测定______等数据,再通过计算得出红色粉末组成.
【交流反思】小红认为红色粉中的铜,有一部分可能是C与Cu2O在高温下反应生成的,写出反应的化学方程式:______ 4Cu+CO2↑
(1)小明先对实验做了如下设想和分析.取少量粉末于烧杯中,向烧杯中加入过量的稀硫酸,则实验中可能出现的现象与对应结论如下表所示(表中未列完所有情况).请你帮助完成.
| 烧杯中可能出现的现象 | 结论 |
| ①有黑色不溶物,无气泡逸出,溶液呈无色 | 结论:只含______ |
| ②______ | 结论:含C、CuO |
| ③______ | 结论:含C、Fe |
【查阅资料】①Cu、Cu2O都是红色固体;
②2CuO+C
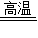 2Cu+CO2↑,4CuO
2Cu+CO2↑,4CuO 2Cu2O+O2↑
2Cu2O+O2↑③CO+Cu2O
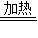 2Cu+CO2,Cu2O+2HCl=CuCl2+Cu+H2O
2Cu+CO2,Cu2O+2HCl=CuCl2+Cu+H2O【猜想】生成的红色粉末究竟是什么?请你和小方一起完成下列猜想:
猜想①Cu; 猜想②Cu2O; 猜想③______.
【设计实验】小方同学设计了一个简单实验很快排除了猜想①,请你帮助他完成下表:
| 实验步骤 | 现象 | 结论 |
| ______ | ______ | 猜想①不正确 |

①取红色粉末样品的质量20克; ②测出反应前B装置的总质量为210.0克;
③反应很长时间后测得B装置的总质量为214.4克;④通过计算确定红色粉末的组成.
根据上述实验,回答下列问题:
Ⅰ.实验开始时,先通CO后称量B装置的总质量,再加热,实验目的是______
A.排尽装置内空气,防止加热发生爆炸
B.防止装置内的空气影响测量结果
C.防止液体倒流到硬质玻璃管中
Ⅱ.C装置的作用是______.
Ⅲ.为防止实验中尾气对大气的污染,可以对尾气进行收集,现提供水槽和集气瓶,还需一种仪器是______.
Ⅳ.请你根据以上数据通过计算,得出红色粉末组成是______.
Ⅴ.不改变装置和药品,你还可以通过测定______等数据,再通过计算得出红色粉末组成.
【交流反思】小红认为红色粉中的铜,有一部分可能是C与Cu2O在高温下反应生成的,写出反应的化学方程式:______ 4Cu+CO2↑