题目内容
 46、等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,请回答:
46、等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,请回答:(1)M、N两种金属中较活泼的是
M
;相对原子质量较大的是
N
.(2)分析图中的两条曲线,从还能得到哪些结论:
等质量的M N,M产生的氢气比N多
.分析:金属可以与酸反应生成氢气,金属的性质越活泼,反应的速度越快,在坐标中就是看斜率,斜率越大,反应速度越快,价态相同的金属与足量的酸反应,相对原子质量大的产生氢气的质量小.
解答:解:(1)从坐标中可以看出,横坐标表示时间,纵坐标表示氢气的质量,则斜率的大小表示反应的速度,M的斜率大,则M的反应速度快,故M比N活泼,价态相同的金属与足量的酸反应,相对原子质量大的产生氢气的质量小,从坐标中可以看出,N产生的氢气少,故N的相对原子质量大,所以本题答案为:M,N;
(2)从图中可以看出,M比N产生的氢气多,所以本题答案为:等质量的M N,M产生的氢气比N多.
(2)从图中可以看出,M比N产生的氢气多,所以本题答案为:等质量的M N,M产生的氢气比N多.
点评:本题考查了金属与酸反应产生氢气的多少和快慢问题,完成此题,可以依据平时解题时积累的规律进行,所以要求同学们对平时的一些规律性知识仔细识记,能够灵活应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 18、等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )
18、等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( ) 20、等质量的M、N两种金属,分别与相同质量分数、等质量的稀盐酸反应成生氢气质量和反应时间的关系如图所示.
20、等质量的M、N两种金属,分别与相同质量分数、等质量的稀盐酸反应成生氢气质量和反应时间的关系如图所示.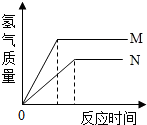 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是 等质量的M、N两种金属,分别与足量的相同浓度的稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述中正确的是( )
等质量的M、N两种金属,分别与足量的相同浓度的稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述中正确的是( )