题目内容
【题目】A~H是初中化学常见的8种物质,其中C不含碳元素,G是黑色固体,相关物质在一定条件下转化关系如图: 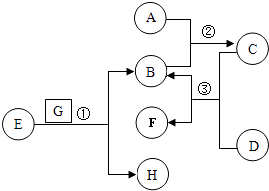
(1)②的反应类型是;反应①的化学方程式为 , 反应③的化学方程式为 .
(2)反应②的化学方程式为 , 实验现象是 .
(3)上述物质中属于氧化物的是(填字母代号).
【答案】
(1)化合反应;2H2O2 ![]() 2H2O+O2↑;2HCl+Ca(OH)2=CaCl2+2H2O
2H2O+O2↑;2HCl+Ca(OH)2=CaCl2+2H2O
(2)CaO+H2O=Ca(OH)2;块状的氧化钙逐渐变成粉末状固体,放出大量的热
(3)GEBA
【解析】解:此题开放性较强,主要是利用其中C不含碳元素,G是黑色固体的信息进行合理的猜想,由图示知E在黑色固体的作用下可以分解生成B和H,因此可以猜想此过程是双氧水的分解反应,由于双氧水分解可以生成水和氧气,所以如果B是水时,则A可以是氧化钙,两者反应可以生成氢氧化钙C,D如果是盐酸,则CD能发生中和反应生成水B和氯化钙F,则也可知H是氧气;(1)②的反应是氧化钙与水生成氢氧化钙的过程,反应物是两种生成物是一种,故是化合反应,反应①是双氧水分解的反应方程式为:2H2O2 ![]() 2H2O+O2↑;反应③氢氧化钙和盐酸的中和反应,方程式为:HCl+Ca(OH)2=CaCl2+H2O;(2)反应②是氧化钙和水的反应,化学方程式为CaO+H2O=Ca(OH)2实验的现象是块状的氧化钙逐渐变成粉末状固体,放出大量的热;(3)氧化物是含有氧元素且一共含有两种元素的化合物,故水、双氧水、氧化钙二氧化锰均是氧化物;所以答案是:(1)化合反应;2H2O2
2H2O+O2↑;反应③氢氧化钙和盐酸的中和反应,方程式为:HCl+Ca(OH)2=CaCl2+H2O;(2)反应②是氧化钙和水的反应,化学方程式为CaO+H2O=Ca(OH)2实验的现象是块状的氧化钙逐渐变成粉末状固体,放出大量的热;(3)氧化物是含有氧元素且一共含有两种元素的化合物,故水、双氧水、氧化钙二氧化锰均是氧化物;所以答案是:(1)化合反应;2H2O2 ![]() 2H2O+O2↑;2HCl+Ca(OH)2=CaCl2+2H2O;(2)CaO+H2O=Ca(OH)2;块状的氧化钙逐渐变成粉末状固体,放出大量的热;(3)GEBA;
2H2O+O2↑;2HCl+Ca(OH)2=CaCl2+2H2O;(2)CaO+H2O=Ca(OH)2;块状的氧化钙逐渐变成粉末状固体,放出大量的热;(3)GEBA;