题目内容
【题目】某化学兴趣小组进行“CO还原氧化铁”的实验(如图),待红色氧化铁完全变成黑色粉末时停止加热,继续通入CO冷却到室温.为检验生成物是否全部为铁粉,他们取出适量的黑色粉末用磁铁验证,发现黑色粉末全部能被磁铁吸引.
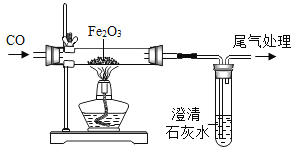
【提出问题】CO还原氧化铁后所得黑色粉末全部是铁粉吗?
【查阅资料】查阅到的相关资料:
(1)CO与氧化铁在570℃以上时,依次发生下列3个反应:
3Fe2O3+CO![]() 2Fe3O4+CO2 Fe3O4+CO
2Fe3O4+CO2 Fe3O4+CO![]() 3FeO+CO2 FeO+CO
3FeO+CO2 FeO+CO![]() Fe+CO2
Fe+CO2
(2)在铁的氧化物中,仅有氧化铁是红色(其余皆是黑色),仅有氧化亚铁在空气中会很快被氧化成氧化铁,仅有四氧化三铁具有磁性.且四氧化三铁不溶于酸、不与酸反应。
【猜想与假设】请你结合课本知识和查到的资料信息,对黑色粉末的组成提出猜想.
猜想①:黑色粉末全部是铁粉;
猜想②:黑色粉末全部是四氧化三铁;
猜想③:黑色粉末________________________.
【实验与结论】请你设计实验验证猜想(假设各组分均能被检出).
A.取样装入试管,_________________,则猜想①正确.
B.取样装入试管,_________________,则猜想②正确。
C.取样装入试管,_________________,则猜想③正确
【反思与拓展】
(1)做“CO还原氧化铁”实验,如何操作才能确保氧化铁被完全还原成铁粉?请你提出1条建议:___________________________.
(2)据报道,大型超市的食品密封包装盒的透明盖内放有少量的氧化亚铁,一旦密封包装破损氧化亚铁就会变为______色,这样售货员就能及时发现.请写出氧化亚铁在空气中自然变色的化学方程式:_________________.
【答案】铁与四氧化三铁的混合物黑色粉末完全溶解并有气泡生成黑色粉末没有溶解无气泡生成黑色粉末部分溶解并有气泡生成控制温度达到570℃以上红4FeO+O2=2Fe2O3
【解析】
【猜想与假设】由于铁与四氧化三铁均能被磁铁吸引,所以黑色固体的成分可能是:全部是铁;全部是四氧化三铁;或者是两者的混合物;
【实验与结论】依据铁能与盐酸反应生成氢气,而四氧化三铁不能与盐酸反应对实验进行设计即可;
【反思与拓展】(1)根据题干中的信息“CO与氧化铁在570℃以上时,依次发生下列3个反应”分析解答;
(2)依据氧化铁的颜色以及题中的信息分析解答;
解:【猜想与假设】由于铁与四氧化三铁均能被磁铁吸引,而该黑色粉末全部能被磁铁吸,所以黑色固体的成分可能是:①全部是铁;②全部是四氧化三铁;③两者的混合物;
【实验与结论】因为铁能与盐酸反应生成氢气,而四氧化三铁不能与盐酸反应,所以①取适量黑色粉末加入足量稀盐酸,黑色粉末完全溶解并有气泡生成,说明该黑色固体全部为铁;②取适量黑色粉末加入足量稀盐酸,黑色粉没有溶解,说明该黑色固体全部是四氧化三铁;③取适量黑色粉末加入足量稀盐酸,黑色粉末部分溶解且有气体放出,则该黑色固体为铁与四氧化三铁的混合物;
【反思与拓展】(1)由于“CO与氧化铁在570℃以上时,依次发生下列3个反应”并最终生成单质的铁,所以要确保氧化铁被完全还原成铁粉,则应控制温度在570℃以上;
(2)依据由于氧化铁的颜色是红色的,所以黑色的氧化亚铁被氧化为氧化铁时,固体会变成红色,反应的方程式为4FeO+O2=2Fe2O3;
故答案为:【猜想与假设】铁与四氧化三铁的混合物.
【实验与结论】取适量黑色粉末加入足量稀盐酸,黑色粉末完全溶解并有气泡生成;
取适量黑色粉末加入足量稀盐酸,黑色粉没有溶解;
取适量黑色粉末加入足量稀盐酸,黑色粉末部分溶解;
【反思与拓展】
(1)控制温度达到570℃以上.
(2)红;4FeO+O2=2Fe2O3.