题目内容
将一枚生锈的铁钉(主要成份是Fe2O3)放入试管中,滴入稀盐酸,观察到的现象 ,写出反应的化学方程式 ;过一段时间后观察到的现象 ,写出反应的化学方程式 .
考点:酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:氧化铁能和稀盐酸反应生成氯化铁和水,氯化铁溶液是黄色的;
铁能和稀盐酸反应生成氯化亚铁和氢气.
铁能和稀盐酸反应生成氯化亚铁和氢气.
解答:解:把一枚生锈的铁钉放入试管中,滴入稀盐酸,观察到铁锈溶解,溶液变成黄色,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;
过一段时间后观察到产生气泡,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故填:铁锈溶解,溶液变成黄色;Fe2O3+6HCl═2FeCl3+3H2O;产生气泡; Fe+2HCl═FeCl2+H2↑.
过一段时间后观察到产生气泡,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故填:铁锈溶解,溶液变成黄色;Fe2O3+6HCl═2FeCl3+3H2O;产生气泡; Fe+2HCl═FeCl2+H2↑.
点评:酸具有一些相似的化学性质,例如能使石蕊试液变红色,能和某些金属单质、某些金属氧化物、某些盐、碱反应生成相应的物质.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案
相关题目
下列有关说法中,正确的是( )
| A、缺锌会使儿童发育停滞,智力低下 |
| B、分子可以再分,而原子不能再分 |
| C、稀有气体不能与其他物质发生任何化学反应 |
| D、液氮不可以用于医疗手术 |
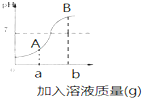 向一定质量的稀硫酸中逐滴加入氢氧化钡溶液,直至过量.如图横坐标表示加入氢氧化钡溶液的质量,根据图线判断,纵坐标可能表示( )
向一定质量的稀硫酸中逐滴加入氢氧化钡溶液,直至过量.如图横坐标表示加入氢氧化钡溶液的质量,根据图线判断,纵坐标可能表示( )| A、硫酸钡沉淀的质量 |
| B、溶液中溶剂的质量 |
| C、溶液中溶质的质量 |
| D、溶液的pH |
实验室有一包白色物质,可能含有碳酸钠、硫酸钾、氯化钡、氯化钠中的一种或几种,小金同学现做了如下实验:取少量白色固体加足量的水溶解,过滤得沉淀和无色溶液.然后向所得沉淀加入少量的稀硝酸,沉淀有部分溶解,并有气体产生; 向滤液中滴入硝酸银溶液,产生白色沉淀.根据上述实验现象和描述,你认为白色固体中( )
| A、一定存在氯化钡、硫酸钾、碳酸钠,可能存在氯化钠 |
| B、一定存在氯化钡、碳酸钠,可能存在硫酸钾、氯化钠 |
| C、四种物质氯化钡、氯化钠、硫酸钾、碳酸钠都一定存在 |
| D、一定存在氯化钡、碳酸钠,一定不存在硫酸钾,可能存在氯化钠 |
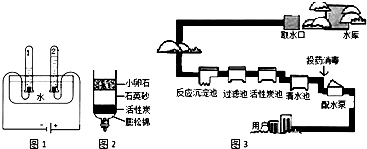 水是生命之源,是人类最宝贵的资源,所以人们要有关心水、爱护水、节约水的意识.请根据下列情况回答问题:
水是生命之源,是人类最宝贵的资源,所以人们要有关心水、爱护水、节约水的意识.请根据下列情况回答问题: