题目内容
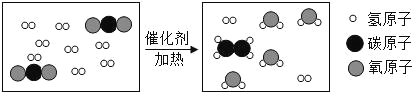
【题目】某小组对H2O2溶液制取氧气进行了如下探究:
(探究一):探究不同催化剂对H2O2分解快慢的影响
该小组采用了如下图所示装置进行实验,实验中催化剂均为0.4g,H2O2溶液浓度均为10%20mL,并用C装置测量收集到50mL水时的某项数据,经计算后的数据如下表:
催化剂种类 | 气体产生速率(mL/s) |
二氧化锰 | 3.5 |
氧化铜 | 4.5 |
活性炭 | 5.8 |
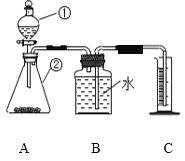
(1)检查A装置气密性的方法是:用弹簧夹夹住A装置右侧导气管,打开①的两个活塞,向其中加水,一段时间后,若____,则气密性良好。
(2)从实验数据可知:相同条件下表中催化剂的催化效果由强到弱依次为____。
(3)该探究实验中,需要测定的数据是___。
(4)当量筒中收集到50mL水时,双氧水分解出的氧气体积实际小于50mL,原因是___。
(探究二):探究H2O2溶液浓度对分解速率的影响
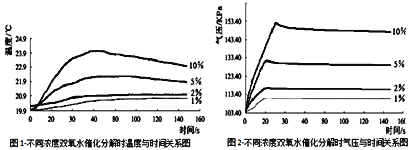
如图:在250mL三颈瓶中,加入MnO2均为0.5g,在恒压漏斗中加入不同浓度的H2O2溶液各20mL分别进行实验。并用温度传感器测量并绘制出瓶内温度与时间关系图。如图1所示。再将该装置的三颈瓶浸入水浴池中(该池可使瓶内的溶液温度恒定在20℃),用上述实验中相同量的各物质重复上述实验,用气压传感器测量并绘制出瓶内气压与时间关系图。如图2所示。

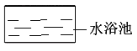
(5)由图1知道:H2O2溶液分解时会___热量(填“放出”或“吸收”)。
(6)由图2知道: H2O2溶液浓度越高,其分解反应速率越____(填“快”或“慢”),以10%H2O2溶液为例,25S后三颈瓶内气压由高缓慢降低的原因是___。
(探究三):探究过氧化氢消毒液的标签
下图是过氧化氢消毒液的标签,结合标签中的信息,请回答:

(7)为什么该消毒液要放在避光、阴凉处保存?请用文字或符号表达式说明___。
(8)该瓶消毒液中至少含有____g过氧化氢,这些过氧化氢中含有的氧元素与____g氧化亚铁中含有的氧元素质量相等。
【答案】一段时间后,漏斗中的水不滴下(或漏斗下管口有水柱) 活性炭>CuO>MnO2 收集50mL氧气所需的时间 装置中存在少量的空气 放出 快 20s反应结束,放热停止,但随着装置散热,温度会下降,使得三颈瓶内气压开始缓慢减小 过氧化氢![]() 水+氧气或H2O2
水+氧气或H2O2![]() H2+O2 3.4g 14.4g
H2+O2 3.4g 14.4g
【解析】
(1)检查A装置气密性的方法是夹住右侧导气管,打开①的两个活塞,向其中加水,若一段时间后,水不滴下(或漏斗下管口有水柱),则气密性良好;
(2)实验数据可知气体产生速率越快催化效果越好,所以分析表格中数据,可以得出相同条件下表中催化剂的催化效果依次为活性炭>CuO>MnO2;
(3)为完成此探究,需要测定的数据为收集50mL氧气所需的时间;
(4)装置中存在少量的空气,所以当量筒中收集到50mL水时,双氧水分解出的氧气体积小于50mL;
(5)由图4可知,随着过氧化氢的分解,温度升高,这说明了H2O2溶液分解时会放出热量;
(6)根据数据可知H2O2溶液浓度越高,反应速率越快,以10%H2O2溶液为例,三颈瓶内气压由高缓慢降低的原因是反应结束,温度下降,气体也因冷却而收缩,使得三颈瓶内气压开始缓慢减小;
(7)过氧化氢分解生成水和氧气,在催化剂或加热条件下反应较快,文字表达式为过氧化氢![]() 水+氧气,符号表达式为H2O2
水+氧气,符号表达式为H2O2![]() H2+O2。
H2+O2。
(8)100mL=0.1L,该瓶消毒液中至少含有过氧化氢的质量为:34.0g/L×0.1L=3.4g;这些过氧化氢中含有的氧元素为3.4g×![]() =3.2g;对应的氧化亚铁的质量为
=3.2g;对应的氧化亚铁的质量为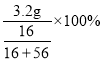 =14.4g。
=14.4g。

【题目】小俊在实验室测定空气中氧气的含量。
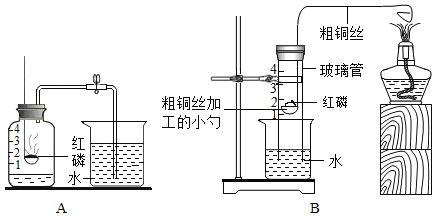
(1)小俊利用图A所示装置实验时,取下橡胶塞,点燃红磷迅速伸入集气瓶中并塞紧橡胶塞,打开止水夹前看到的现象是____________,涉及到化学方程式为_____________;
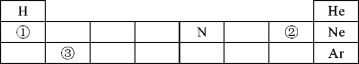
(2)在实验室中小俊发现了如下图B所示的改进装置,并在装置的使用说明上阅读到了白磷和红磷的相关知识:
红磷 | 紫红或略带棕色的固体 | 难溶于水,密度比水大 | 200℃以上着火(约260℃) | 燃烧时产生白烟,烟有毒。化学性质比白磷差,在常温下稳定,难与氧反应。 |
白磷 | 白色或浅黄色半透明性固体。 | 不溶于水,密度比水大 | 在湿空气中约30℃着火,在干燥空气中则稍高。 | 有毒。人的手温就容易使白磷燃烧,所以取用时必须用镊子,存放多在冷水中。 |
①B装置的优点是_____________(只写一点);
②装置中粗铜丝的作用是___________;
③从理论上分析,玻璃管内液面最终将上升至___________处(填1、2、3、4);
④在老师的协助下,小俊用B装置也做了测定了空气中氧气的含量,发现实验测结果液面偏低,其原因可能是__________。
【题目】某同学对生铁的组成进行研究.称取生铁样品40g,把500g稀硫酸分5次加入样品中,测得实验数据见下表:(生铁中的杂质不溶于水,也不和稀硫酸反应)
实验序号 | 加入稀硫酸的质量/g | 剩余固体的质量/g |
第1次 | 100 | 28.8 |
第2次 | 100 | 17.6 |
第3次 | 100 | 6.4 |
第4次 | 100 | m |
第5次 | 100 | 1.2 |
(1)第4次剩余固体的质量m= g.
(2)该生铁样品中铁的质量分数为 .
(3)计算所用稀硫酸的溶质质量分数.