题目内容
还原铁粉是化工生产及实验室中常用的还原剂。工业上以绿矾(FeSO4·7H2O)为原料制备还原铁粉的工艺流程见图1。
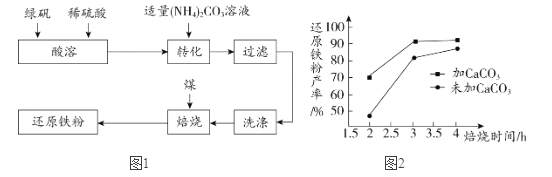
(1)转化时,将(NH4)2CO3溶液加入到FeSO4溶液中,目的是制得FeCO3。
(2)将FeCO3浊液暴露在空气中,反应的化学方程式为: ,其中X是_____。
,其中X是_____。
(3)焙烧时,发生的反应有:① ; ②
; ②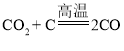 ;③
;③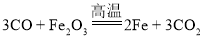 ,其中属于分解反应的是________(填序号)。
,其中属于分解反应的是________(填序号)。
(4) 在焙烧过程中需加入CaCO3进行脱硫处理。图2为加CaCO3和不加CaCO3对还原铁粉产率的影响,由图可以得出的结论是_____________。
 轻松课堂单元期中期末专题冲刺100分系列答案
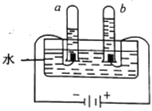
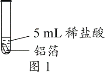
轻松课堂单元期中期末专题冲刺100分系列答案化学小组同学用图1装置探究铝与盐酸的反应。将未去除表面氧化膜的铝箔放入稀盐酸中,刚开始反应现象不明显,一段时间后反应比较剧烈,产生大量气泡,出现灰色沉淀。
(查阅资料)
①铝粉在颗粒较小时为灰黑色;铝既能与酸反应,又能与碱反应,且反应均生成氢气。
②氯化铝固体为白色颗粒或粉末,易溶于水和乙醇。
③氧化铝与盐酸反应的化学方程式为: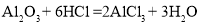 。
。
(实验一)探究灰色固体的成分
实验序号 | 1-1 | 1-2 | 1-3 | 1-4 |
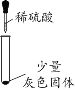
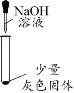
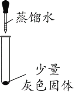
实验操作 |
|
|
|
|
实验现象 | 有微量气泡产生,固体溶解 | 有少量气泡产生,固体溶解 | ____________ | 固体部分溶解 |
(实验二)探究盐酸浓度对灰色固体产生量的影响
取0.09 g铝箔和5 mL不同浓度的稀盐酸,用图1装置进行实验。
实验序号 | 盐酸浓度 | 实验现象 |
2-1 | 4.0% | 刚开始反应现象不明显,一段时间后缓慢反应,然后反应比较剧烈,有大量气泡产生,出现灰色沉淀 |
2-2 | 2.8% | 先是看不到反应现象,一段时间后缓慢反应,然后慢慢地反应比较剧烈,有大量气泡产生,出现少量灰色沉淀 |
2-3 | 2.1% | 3~4小时后明显有气泡产生,反应慢慢地比较快些,试管底部出现少量灰色沉淀 |
2-4 | 1.4% | 反应更慢,出现极少量的灰色沉淀 |
(解释与结论)
(1)铝与盐酸反应的化学方程式为___________。
(2)图1所示实验中,刚开始反应现象不明显,一段时间后才看到有气泡产生的原因是________。
(3)由实验________(填实验序号)可以判断灰色固体中含有铝。
(4)由实验1-4可知,灰色固体中还含有氯化铝。实验1-3的现象是_________。
(5)实验二的结论是__________。
(反思与交流)
(6)为了进一步探究灰色沉淀的出现是否与盐酸中的Cl-有关,可以将稀盐酸换成______进行图1所示实验。
菠菜、苋菜、空心菜、芥菜、韭菜等蔬菜中含有丰富的草酸(H2C2O4),请预测草酸的化学性质,说明预测的依据,并设计实验验证。经查阅资料,部分化合物的溶解性如下:
物质 | H2C2O4 | Na2C2O4 | CaC2O4 | CuC2O4 |
在水中溶的溶解性 | 易溶于水的无色溶液 | 易溶于水的无色溶液 | 难溶于水的白色固体 | 难溶于水的浅蓝绿色固体 |
限选试剂是:H2C2O4溶液、稀盐酸、NaOH溶液、CaCl2溶液、Na2CO3溶液、酚酞溶液、铜片、镁条。
预测 | 预测的依据 | 验证预测的实验操作与预期现象 |
①能与活泼金属反应。 | H2C2O4溶液中含有H+ | 取少量草酸溶液于试管中,_____,如果观察到_____,则预测成立。 |
②能与_____(填物质类别)反应。 | _____ | _____,如果观察到_____,则预测成立。 |
③能与_____(填物质类别)反应。 | _____ | _____,如果观察到_____,则预测成立。 |