��Ŀ����
����Ŀ���ҹ��Ŵ���¯��ʯ����Ҫ�ɷ֣�ZnCO3������ͭ����Ҫ�ɷ֣�Cu2O����ľ̿��Ϊԭ��ֵ������ͭ��ͭ��п�ĺϽ�����ƻƽ𣩣�������������ͼ1�� 
�ش��������⣺
��1����ͭ����Ҫ�ɷ�Cu2O��ͭԪ�صĻ��ϼ�Ϊ
��2������ʱ����������Ҫ��Ӧ��ѧ����ʽΪ����ZnCO3 ![]() ZnO+CO2������2ZnO+C
ZnO+CO2������2ZnO+C ![]() 2Zn+CO2����������ͭ��ľ̿�۷�Ӧ��
2Zn+CO2����������ͭ��ľ̿�۷�Ӧ��
��3��ij��ȤС��ͬѧ��������Ӧ���ɵ�����A�ijɷֽ����о��� ��������⡿���ɵ��������Ƿ���һ����̼��
��ȤС��ͬѧ����ͼ2��ʾ��װ�ý���ʵ�飬�����ɵ�����ɷֽ���̽����
��ʵ�������ۡ�
�ٴ�K������ͨ�����ĵ���һ��ʱ�䣮
�ڹر�K��������һ���¶�ʹ�������е�¯��ʯ����ͭ��ľ̿�۷�Ӧ���������ռ�������Ʒ��
������ȥ������Ʒ�еĶ�����̼������ʣ�������ռ��ڼ���ƿ�У�����ͼ3װ������Ϊ�������� �� 
��ʵ����֤��������������̼���������Ʒ�����Ȼ��ͼ2��ʾ��װ�ý���ʵ�飬A�еĹ���Ӧѡ�� �� B����ҺΪ����ʯ��ˮ����A�к�ɫ��������˺�ɫ��B�г���ʯ��ˮ �� �仯ѧ����ʽΪ �� ��˵��������Ʒ�к���һ����̼��
��ʵ�鷴˼������ʵ���У������ɵ������к���һ����̼����Ӧʱ����̼����Ԫ�ص�������������ڡ��������ڡ���С�ڡ���3��8��
��4����һ��ȤС��ͬѧ��������Ӧ���ɵĹ���ɷֽ������о��� �ټ�ͬѧ˵��ͭ��п�Ͻ���ͬѧ˵�����ǽ�
������ͬѧ������ͬѧ�IJ²⣮�������� ��
��Ϊ�ⶨ�û�ͭ��ͭ��п�Ͻ���ͭ������������ij��ȤС��ȡ20g��ͭ��Ʒ����ʢ��200gϡ������ձ��У�ǡ����ȫ��Ӧ������ձ���ʣ�����ʵ�������Ϊ219.8g���û�ͭ��Ʒ��ͭ����������Ϊ �� ������������0.1%��
���е���ȤС����ͼ4װ�òⶨ��ͭ��ͭ���������������й��ڸ�ʵ���˵����ȷ����
A����Һ©�����Թܼ���ܽ���ʹҺ��˳���µε�����
B����ʵ����ϡ����㣬�����·�Һ©���Ϸ�����Ƥ������
C���òⶨ����Ҫ����������Ʒ�����ʹ��¶ȡ�ѹǿ���������ܶ�
D��ʵ�����ʱ������ȴ�����²��������ܻ�������������Һ����ƽ�ٶ���
��5����չ���� ��ij��ѧС����һ����AgNO3��Al��NO3��3�Ļ����Һ����ͭ�ۺ�п�ۣ���ַ�Ӧ����ˣ��õ���Һ�����ң���ͼ5��ʾ����
a����Һ����һ������Al��NO3��3��Zn��NO3��2
b����������һ������Ag�����ܺ���Cu��Zn
c������Һ������ɫ������Һ��һ������Al��NO3��3��Zn��NO3��2��Cu��NO3��2
d����������ϵμ����������ݲ���������Һ����һ��û��AgNO3��Cu��NO3��2
��������˵����ȷ�ĸ���Ϊ
A��1�� B��2�� C��3�� D��4��
�����÷Ͼɵ��ͭñ����Cu��Zn����ȡCu�����õ�ZnSO4��Һ����Ҫ������ͼ6������֪���ٷ�Ӧ��������ȥ����2Cu+2H2SO4+O2 ![]() 2CuSO4+2H2O����
2CuSO4+2H2O����
a����ҺA����C����������Ԫ�أ����̢��еķ�������� ��
b����д��������з�����Ӧ�Ļ�ѧ����ʽ�� ��
���𰸡�
��1��+1
��2��2Cu2O+C ![]() 4Cu+CO2��
4Cu+CO2��
��3��C������ͭ������ǣ�CO+CuO ![]() Cu+CO2������
Cu+CO2������
��4����ѧ��Ӧǰ��Ԫ�ص�����䣻67.5%��CD
��5��D��ͭ��п�����ˣ�Zn+H2SO4�TZnSO4+H2��
���������⣺��1����Cu2O��ͭԪ�صĻ��ϼ�Ϊx������2x+����2��=0��x=+1�����+1����2������ʱ��������ͭ��̼���·�Ӧ����ͭ�Ͷ�����̼�����2Cu2O+C ![]() 4Cu+CO2������3��������ȥ������Ʒ�еĶ�����̼������Ҫͨ������������Һ��Ҫ��ʣ�������ռ��ڼ���ƿ�У�����Һ��Ҫ�ӳ����ų�����ͼ3װ������Ϊ�������� C�����C�� ��ʵ����֤��A�к�ɫ��������˺�ɫ��˵��A�еĹ���Ӧѡ�õ�������ͭ��һ����̼������ͭ��Ӧ����ͭ�Ͷ�����̼����B�г���ʯ��ˮ����ǣ��仯ѧ����ʽΪ CO+CuO
4Cu+CO2������3��������ȥ������Ʒ�еĶ�����̼������Ҫͨ������������Һ��Ҫ��ʣ�������ռ��ڼ���ƿ�У�����Һ��Ҫ�ӳ����ų�����ͼ3װ������Ϊ�������� C�����C�� ��ʵ����֤��A�к�ɫ��������˺�ɫ��˵��A�еĹ���Ӧѡ�õ�������ͭ��һ����̼������ͭ��Ӧ����ͭ�Ͷ�����̼����B�г���ʯ��ˮ����ǣ��仯ѧ����ʽΪ CO+CuO ![]() Cu+CO2 �� �������ͭ������ǣ�CO+CuO
Cu+CO2 �� �������ͭ������ǣ�CO+CuO ![]() Cu+CO2��
Cu+CO2��
��ʵ�鷴˼�����ɵ������к���һ����̼����Ӧʱ����̼����Ԫ�ص������ȴ���3��8��������ڣ���4���ٸ��������غ㶨�ɣ���ѧ��Ӧǰ��Ԫ�ص�����䣬�ʲ��������ɽ𣬹����ѧ��Ӧǰ��Ԫ�ص�����䣮�ڲ�������������Ϊ��20g+200g��219.8g=0.2g
��п������Ϊx
Zn+H2SO4�TZnSO4+ | H2�� |
65 | 2 |
x | 0.2g |
![]()
x=6.5g
�ʸû�ͭ��Ʒ��ͭ����������Ϊ�� ![]() =67.5%�����67.5%��
=67.5%�����67.5%��
����ͼ4װ�òⶨ��ͭ��ͭ����������ʱ��A����Һ©�����Թܼ���ܳ���ʹҺ��˳���µε����ã��������ܷ�����ã�����B����ʵ����ϡ����㣬�������·�Һ©���Ϸ�����Ƥ�����ӣ����������װ��©��������C���òⶨ����Ҫ����������Ʒ�����ʹ��¶ȡ�ѹǿ���������ܶȣ���ȷ��D��ʵ�����ʱ������ȴ�����²��������ܻ�������������Һ����ƽ�ٶ�������ȷ�����CD����5����ij��ѧС����һ����AgNO3��Al��NO3��3�Ļ����Һ����ͭ�ۺ�п�ۣ�п��ͭ�������ĺ��棬��������������Ӧ��ֻ������������Ӧ��������п������������Ӧ��
a��п�Ȳ��뷴Ӧ������Һ����һ������Al��NO3��3��Zn��NO3��2 �� ��ȷ��
b����������һ������Ag�����ܺ���Cu��Zn����ȷ��
c������Һ������ɫ������Һ��һ������Al��NO3��3��Zn��NO3��2��Cu��NO3��2����ȷ��
d����������ϵμ����������ݲ�������пʣ�࣬����Һ����һ��û��AgNO3��Cu��NO3��2 �� ��ȷ��
��˵����ȷ�ĸ���Ϊ4�������D��
�� 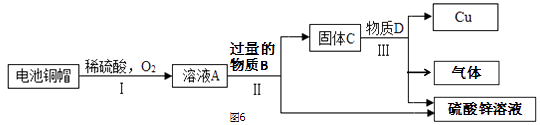
a����ҺA����C������ͭ��п����Ԫ�أ����̢��з���õ����ǹ����Һ�壬�÷�������ǹ��ˣ�������ˣ�
b���������п��ϡ���ᷴӦ��������п��������������Ӧ�Ļ�ѧ����ʽ��Zn+H2SO4�TZnSO4+H2�������Zn+H2SO4�TZnSO4+H2����
�����㾫����������Ҫ�����˹��˲�����ע������ͽ������ϵ�ѡ�����ݵ����֪ʶ�㣬��Ҫ���չ��˲���ע�������һ���������͡������������˺���Һ��Ȼ���ǵĿ���ԭ����:�ٳн���Һ���ձ����ɾ����㵹Һ��ʱҺ�������ֽ��Ե����ֽ���𣻺�ɫ������ͨ��ָ�����̡��������ǵĺϽ��ؽ�������ͭ��п��Ǧ�ȣ���ɫ��������������ơ�þ�����ȣ���ɫ������ͨ����ָ����ɫ�����������������������ȷ�����⣮

����Ŀ����ͼ���������˵����ʿ������Ӧ�������ĸ�ѡ���У�����Ҫ����ǣ� ��
�� | �� | �� | �� | |
A | Fe2O3 | CO | O2 | C |
B | HCl | Cu | AgNO3 | Zn |
C | CaCO3 | HCl | Cu | O2 |
D | H2 | O2 | Fe | HCl |

A.A
B.B
C.C
D.D