题目内容
【题目】金属氢化物如氢化钙(CaH2)、氢化钠(NaH)是重要的制氢剂,与水接触 时,分别发生如下反应:CaH2+2H2O═Ca(OH)2+2H2↑,NaH+H2O═NaOH+H2↑。
(1)若用 25g 某氢化钠工业样品可制得氢气 2g,请计算该氢化钠样品的纯度(样品中 NaH 的质量分数)是多少____?
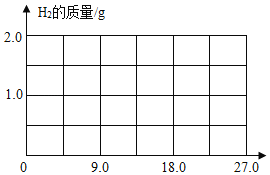
(2)向 25g 上述氢化钠工业样品中逐渐加入水至过量,在图中画出产生氢气的曲线图____。
(3)登山运动员登山时也需通过金属氢化物与水反应获得氢气以提供必须的能量。小红认为,若用 CaH2替代 NaH,有利于登山运动员减轻包袱负担。原因是:____。
【答案】96% 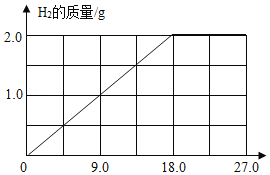 相同质量的CaH2比NaH产生的氢气多;
相同质量的CaH2比NaH产生的氢气多;
【解析】
解:(1)设样品中NaH的质量分数为x,
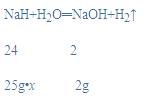
![]()
x=96%;
答:该样品中NaH的质量分数为96%。
(2)氢气的质量逐渐增加,最后不变;故答案为: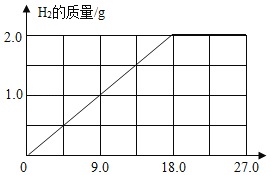 ;
;
(3)小红认为,若用CaH2替代NaH,有利于登山运动员减轻包袱负担;原因是:相同质量的CaH2比NaH产生的氢气多。

【题目】下表是氯化钠、硝酸钾在不同温度时的溶解度。据此判断:下列说法不正确的是
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
硝酸钾 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
A. 氯化钠和硝酸钾的溶解度曲线在20℃~30℃温度范围内会相交
B. 在20℃时, 向68g饱和氯化钠溶液中加入32g水,此时溶液中溶质的质量分数为18%
C. 从含有少量氯化钠的饱和硝酸钾溶液中得到较多的硝酸钾晶体,可采用冷却热饱和溶液使其结晶的方法
D. 分别将20℃时一定质量的饱和氯化钠溶液、饱和硝酸钾溶液升温至40℃,此时硝酸钾溶液中溶质的质量分数大于氯化钠溶液
【题目】请你根据教材中学过的知识完成下表:
实验目的 | 实验操作 | 实验现象 | 得到结论 |
比较空气与呼出的气体中氧气的含量 | ①______________ | ②_____________ | 呼出气体中氧气的含量比空气中氧气的含量低 |
探究蜡烛的物理性质 | 用小刀切一小块蜡烛,投入水中,一段时间,无明显变化 | 蜡烛浮在水面上,一段时间无明显变化 | 蜡烛的硬度较低, ③______________ |
探究火焰各部分温度的高低 |
将一根细木条放入火焰中,约2秒后立即取出 | 木条两侧被烧痕迹最重 | ④______________ |
探究蜡烛燃烧后的产物 (资料) 硫酸铜(CuSO4)是一种白色粉末,具有吸水性,吸水后变为蓝色。 |
| 澄清石灰水变浑浊,白色硫酸铜粉末变为蓝色 | ⑤______________ |
【题目】小明设计了如下图所示的实验装置来证明氧化铜能加快过氧化氢溶液的分解,并与相同条件下![]() 的催化效果做比较,实验时间均以生成
的催化效果做比较,实验时间均以生成![]() 气体为准(即比较反应速率).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
气体为准(即比较反应速率).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
实验序号 | 过氧化氢溶液体积 | 催化剂 | 待测数据 |
① |
| 无 | |
② |
| 氧化铜 | |
③ |
|
|
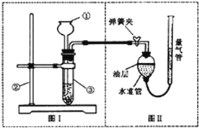
![]() 图中油层的作用是________
图中油层的作用是________
![]() 从设计原理看,实验中的“待测数据”可以是指________.
从设计原理看,实验中的“待测数据”可以是指________.
![]() 为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意________(填字母编号).
为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意________(填字母编号).
![]() .视线与凹液面最低处相平
.视线与凹液面最低处相平
![]() .读数前不能移动量气管和水准管
.读数前不能移动量气管和水准管
![]() .保持水准管静止,待水准管中液面不再上升时,立刻读数
.保持水准管静止,待水准管中液面不再上升时,立刻读数
![]() .读数前应上下移动水准管,待两管液面相平再读数
.读数前应上下移动水准管,待两管液面相平再读数
![]() 如果要进一步探究氧化铜是否是该反应的催化剂,请完成下列实验.
如果要进一步探究氧化铜是否是该反应的催化剂,请完成下列实验.
实验步骤和现象 | 设计这一步骤的目的 |
| 氧化铜能够加快过氧化氢溶液的分解 |
________________ | ________________ |
________________ | ________________ |