题目内容
【题目】黄铜是铜和锌的合金,化学学习小组的同学设计以下实验过程,将回收的黄铜废料进行处理,得到金属铜并制取硫酸锌晶体。
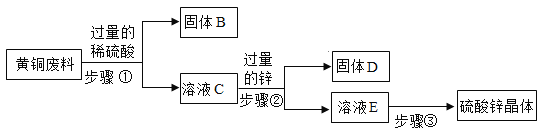
(1)固体B的化学式为_____, 写出步骤①的化学方程式_____。
(2)步骤①、②实验基本操作中玻璃棒的作用是 _____,步骤③实验基本操作的名称是_____。
(3)该流程中,能否根据得到的硫酸锌质量,求出一定质量的黄铜中锌的质量分数? _____(填“能”或“不能”), 原因是_____。
【答案】Cu ![]() 引流 蒸发结晶 不能 步骤②中又加入了锌,加入的锌与过量的稀硫酸反应也生成了硫酸锌
引流 蒸发结晶 不能 步骤②中又加入了锌,加入的锌与过量的稀硫酸反应也生成了硫酸锌
【解析】
(1)黄铜是铜和锌的合金,加入过量的稀硫酸,在金属活动性顺序里,锌位于氢之前,锌能与稀硫酸反应生成硫酸锌和氢气,铜位于氢之后,铜不与稀硫酸反应,故固体B为铜,化学式为Cu;
步骤①为锌和稀硫酸反应生成硫酸锌和氢气,该反应的化学方程式为:![]() ;
;
(2)步骤①、②都实现了固液分离,故该基本操作为过滤,在过滤中玻璃棒的作用是引流;
步骤③由溶液变为硫酸锌晶体,故实验基本操作的名称是蒸发结晶;
(3)不能,因为步骤②中又加入了锌,加入的锌与过量的稀硫酸反应也生成了硫酸锌。

练习册系列答案
相关题目