题目内容
X和Z是由A、B、C三种元素(A、B、C均为1~18号元素)形成的两种化合物.已知元素A在两种化合物中的质量分数分别为29.1%和17.0%,且B、C的质量比在两种化合物中是相同的.已知化合物X的化学式为A2B2C3,z的化学式为A2BxCy.它的溶液跟盐酸混合时有气体和浅黄色沉淀生成,该气体是形成酸雨的主要原因.则元素A是分析:形成酸雨的气体为二氧化硫,浅黄色沉淀 为硫,确定出BC元素种类为硫和氧,根据A在X化合物中质量分数确定出A元素的种类,再根据质量分数确定出xy的原子个数比.
解答:解:Z与盐酸反应生成形成酸雨的气体(即二氧化硫)和浅黄色沉淀,则为单质S,故Z中一定含有硫元素和氧元素,即B为硫元素,C为氧元素,根据X中A的质量分数为29.1%,可知:29.1%=
×100% 求出A=23,故A元素为钠元素,根据Z中A元素的质量分数为17%可知:17%=
×100%,求出2x+y≈14.因为且B、C的质量比在两种化合物中是相同的,所以
=
综上,可得x=4,y=6,故Z的化学式为Na2S4O6
故答案为 Na,S,O,Na2S4O6
| A×2 |
| A×2+32×2+16×3 |
| 23×2 |
| 23×2+32×x+16×y |
| x |
| y |
| 2 |
| 3 |
故答案为 Na,S,O,Na2S4O6
点评:根据反应前后元素种类不变以及反应现象确定出元素种类,再根据质量分数确定原子个数,灵活运用质量分数的计算公式是解答本题关健.

练习册系列答案
相关题目
 学过金属的活动性顺序以后,明明同学对其一系列知识进行了研究.
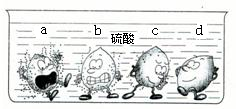
学过金属的活动性顺序以后,明明同学对其一系列知识进行了研究.(1)据下图中的实验现象判断,稀硫酸里a、b、c、d四种金属中,位于氢后面的金属是
(2)将金属Ni、Mn分别放入其他三种金属X、Y、Z的盐溶液中,反应的结果和有无金属析出的情况如右表所示.则它们的金属活动性由强到弱的顺序为(
| X盐溶液 | Y盐溶液 | Z盐溶液 | |
| Ni | 无 | 无 | 有 |
| Mn | 无 | 有 | 有 |
B.Z Ni Y Mn X
C.X Mn Y Ni Z
D.X Mn Ni Y Z
(3)查阅资料:金属在活动性顺序里的位置越靠后,其化合物越不稳定,所以它的氧化物越易被还原.请你写出下列用金属氧化物制取金属的化学方程式:
①金属氧化物加热分解:
②用碳还原金属氧化物:
(4)查阅资料:在金属活动性顺序里,位于氢后面的金属铜在常温下虽然不能与稀盐酸、
稀硫酸反应,但可以与浓硫酸在加热时发生反应,其反应的化学方程式为:
Cu+2H2SO4(浓)?CuSO4+SO2↑+2H2O
反应生成的SO2是一种无色、能溶于水、有刺激性气味的气体.若用该方法制取硫酸铜,应用
(5)请你利用所学知识设计一种以铜、稀硫酸为主要原料制取硫酸铜的方法.(用化学方程式表示)
(6)向12.8g铜中加入40g浓硫酸溶液,恰好完全反应,计算生成SO2的质量(方程式见上)和反应前硫酸溶液中溶质的质量分数.