题目内容
30、某同学在做实验时发现盛放NaOH溶液的试剂瓶口与橡皮塞上常有白色粉末出现,为探究这一白色粉末的成分,他做了以下实验:
(1)取少量白色粉末于试管中,再滴加稀HCl,有气泡产生,由此可推出白色粉末中含有
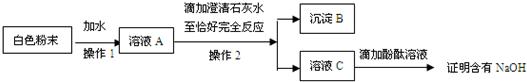
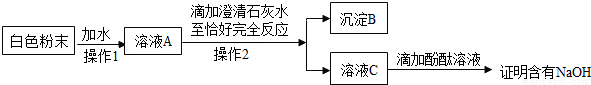
(2)该同学为进一步探究白色粉末是否含有NaOH,设计了如下实验方案: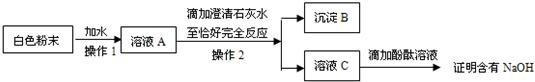
①沉淀B的化学式为
②在操作1中要用到玻璃棒,其作用是
③你认为该同学的这个方案是否正确?
(1)取少量白色粉末于试管中,再滴加稀HCl,有气泡产生,由此可推出白色粉末中含有
Na2CO3
.(2)该同学为进一步探究白色粉末是否含有NaOH,设计了如下实验方案:

①沉淀B的化学式为
CaCO3
.②在操作1中要用到玻璃棒,其作用是
搅拌
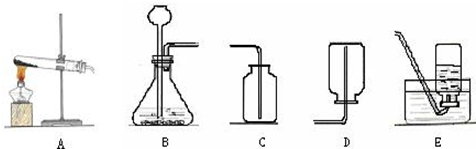
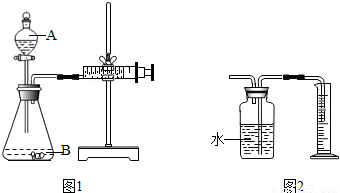
;在操作2中,除要用到铁架台(带铁圈)、烧杯、滤纸、玻璃棒外,还需补充的玻璃仪器是漏斗
.③你认为该同学的这个方案是否正确?
不正确
(填“正确”或“不正确”),理由是Na2CO3与Ca(OH)2反应后也有NaOH生成,因此这个方案不能证明白色粉末中是否含有NaOH
.分析:(1)根据氢氧化钠与二氧化碳反应生成碳酸风传和水,碳酸钠与盐酸反应生成氯化钠、水、二氧化碳的性质回答.
(2)①根据碳酸钠与氢氧化钙反应生成碳酸钙沉淀和水的性质回答.
②根据溶解时玻璃棒的作用和过滤时用的仪器回答.
③根据碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠的性质回答.
(2)①根据碳酸钠与氢氧化钙反应生成碳酸钙沉淀和水的性质回答.
②根据溶解时玻璃棒的作用和过滤时用的仪器回答.
③根据碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠的性质回答.
解答:解:(1)NaOH能与空气中的二氧化碳反应生成碳酸钠和水而变质,向试剂瓶口与橡皮塞上的白色粉末中加入盐酸有气泡,则证明粉末是碳酸钠.
(2)①白色粉末是碳酸钠,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和水,所以沉淀B为碳酸钙,化学式为:CaCO3.
②操作1为溶解,玻璃棒的作用是搅拌,促进溶质溶解;过滤用到的仪器有:铁架台(带铁圈)、烧杯、滤纸、玻璃棒外、漏斗,所以需补充的玻璃仪器是漏斗.
③该同学方案不正确,因为Na2CO3与Ca(OH)2反应后也有NaOH生成,因此这个方案不能证明白色粉末中是否含有NaOH.
故答案为:
(1)Na2CO3;
(2)①CaCO3;②搅拌;漏斗;③不正确;Na2CO3与Ca(OH)2反应后也有NaOH生成,因此这个方案不能证明白色粉末中是否含有NaOH.
(2)①白色粉末是碳酸钠,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和水,所以沉淀B为碳酸钙,化学式为:CaCO3.
②操作1为溶解,玻璃棒的作用是搅拌,促进溶质溶解;过滤用到的仪器有:铁架台(带铁圈)、烧杯、滤纸、玻璃棒外、漏斗,所以需补充的玻璃仪器是漏斗.
③该同学方案不正确,因为Na2CO3与Ca(OH)2反应后也有NaOH生成,因此这个方案不能证明白色粉末中是否含有NaOH.
故答案为:
(1)Na2CO3;
(2)①CaCO3;②搅拌;漏斗;③不正确;Na2CO3与Ca(OH)2反应后也有NaOH生成,因此这个方案不能证明白色粉末中是否含有NaOH.
点评:综合实验涉及知识面广,对学生思维能力要求高,既考查知识的识记、理解、迁移、运用,又考查分析、对比、归纳等思维能力,符合素质教育培养学生能力的要求,是中考方向,对这类题目要重点训练.

练习册系列答案
相关题目