题目内容
(7分)已知A是酸,其浓溶液有脱水性;B为氮肥,C为钾肥,
D为白色不溶于水的固体。它们之间的转化关系如下图: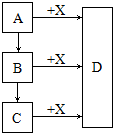
(1)D的名称是 。
(2)A和X反应的化学方程式为: 。
(3)B转化为C的化学方程式为: 。
(4)实验室稀释A的浓溶液操作方法:
。
(1)硫酸钡(1分)
(2)H2SO4+BaCl2==BaSO4↓+2HCl(与硝酸钡反应也可) (2分)
(3)2KOH+(NH4)2SO4==K2SO4+2NH3↑+2H2O (2分)
(4)将浓硫酸沿着烧杯内壁缓缓注入水中,并用玻璃棒不断搅拌。(答到“硫酸倒入水中”得1分,“搅拌”得1分)
解析试题分析:A是酸,其浓溶液有脱水性,所以A为硫酸;A与X反应生成D,D为白色不溶于水的固体,所以D为硫酸钡;B为氮肥,C为钾肥,可以由A转化得到,所以B为硫酸铵,C为硫酸钾,A和X反应的化学方程式为:H2SO4+BaCl2==BaSO4↓+2HCl(与硝酸钡反应也可);B转化为C的化学方程式为:2KOH+(NH4)2SO4==K2SO4+2NH3↑+2H2O;浓硫酸溶于水会放出大量的热,且浓硫酸具有腐蚀性,密度比空气大,所以稀释浓硫酸时,要将浓硫酸沿着烧杯内壁缓缓注入水中,并用玻璃棒不断搅拌。
考点:物质的推断、酸碱盐的化学性质、化学肥料、浓硫酸的稀释

练习册系列答案
相关题目
(5分)根据下表数据,回答下列问题。
| 物质 | 厕所清洁剂 | 白醋 | 食盐水 | 洗涤剂 | 炉具清洁剂 |
| pH | 1 | 3 | 7 | 9 | 12 |
(2)水壶中的水垢,主要成分为碳酸钙和氢氧化镁,用白醋 (填“能”或“不能”)去除。
(3)生活中用洗涤剂清洗餐具上的油污,这种现象属于 。
(4)厕所清洁剂与炉具清洁剂 (填“能”或“不能”)混合使用;由表可知食盐水呈中性,再举出一种呈中性的溶液,如 溶液。

